|
|
Teorii etiopatogenice in SM
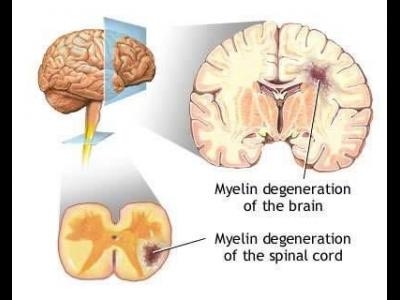
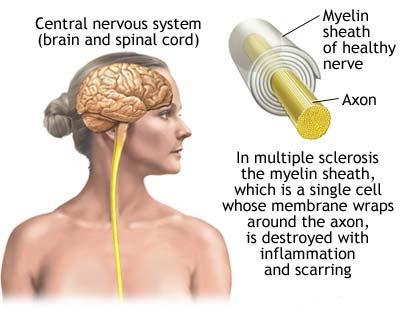
Pentru a ajunge la actualele teorii de patogenitate in SM, trebuie sa trecem in revista cunostintele si informatiile anterioare privitoare la aceasta boala demielinizanta a sistemului nervos central (SNC).
In primul rand, pentru sustinerea concreta a diagnosticului de SM este necesar sa imbinam toate datele aferente: cele clinice (este necesar sa evaluam cazul dupa cel putin doua pusee acute), in care predomina examenul neurologic, completate cu date paraclinice si de laborator.
Un prim caz in istoria medicala, presupus SM a fost cel al lui LUDWIG de SHEDHAM (1380-l433) care a prezentat o boala cu manifestari neurologice in pusee, urmata de perioade de remisiune, care nu ceda la nici un tratament.
AUGUST FREDERIC D ESTE pomenea in scrierile si jurnalul sau despre o boala care a debutat pe fondul unei nevrite optice cu multiple alte manifestari neurologice (incontinenta urinara si fecala) cu evolutie progresiva stadiala.
Primele descrieri ale bolii din punct de vedere al unui medic dateaza intre anii (1828-l835-l838), punandu-se baza mai ales, pe leziunile anatomice (HOOPER; CRUIVEILLIER sau CRASWELL).
Totodata, anatomistii lanseaza prima salva de informatii care vor duce ulterior la nomenclatura acestei boli (scleroza multipla), termenii anglofoni
(multiple sclerosis) sau germanofoni (multiple sklerose), descriind leziuni in pete , sau in insule cu structura caracteristica si de sine statatoare. Autorii francofoni denumesc boala scleroza in placi
Odata leziunea descoperita a intervenit inevitabilul de ce ? trecandu-se la explicatii patogenice.
Prima explicatie ar fi fost teoria vasculara si inflamatorie (1963, RINDFLEISCH).
Urmatoarea explicatie ar fi avut-o teoria infectioasa care s-a pus in cauza odata cu dezvoltarea virusologiei si nici astazi aceasta teorie nu este pe deplin confirmata sau neconfirmata. Un contraargument al acestei teorii ar fi netransmisibilitatea bolii intr-un mediu familial. De exemplu SCHAPIRO si colaboratorii (1962) au gasit numai 8 cupluri care sufereau de SM, pe un studiu de 10.000 de bolnavi cu aceasta boala.
Odata cu dezvoltarea imunologiei si intelegerea complexa a capacitatii de aparare a organismului, cu datele coroborate de laborator si anamnestice, s-a avansat ipoteza unei teorii autoimune.
Unii autori accepta o teorie mixta autoimuno-infectioasa datorita asemanarii unei proteine bazice mielinice (PBM) cu structurile unor virusi.
In sfarsit, studii efectuate asupra gemenilor mono- si dizigoti, au scos la iveala factorul genetic, care este considerat mai mult factor favorizant decat etiologic.
Frecventa cu care celalalt geaman este atins de SM de este de 2,5 pentru cazul monozigotilor (CONFAVREUX, 1991).
Un alt factor ce pledeaza pentru teoria genetica este asociatia intre SM si un anumit genotip, in ceea ce priveste structura moleculara H.L.A. clasa I si II.
Pentru moleculele clasa I-a legatura a fost facuta cu H.L.A. - A3 si B7, iar pentru H.L.A. clasa a II-a, cu subgrupele antigenice DRw15, pentru DRq si DRw6 pentru DQw1. Antigenii DP nu par sa influenteze susceptibilitatea la SCLEROZA MULTIPLA.
Totusi, aceasta asociere nu trebuie luata drept model de referinta, pentru ca s-a observat o distributie pe etnii a asocierilor SM, cu diferite H.L.A. clasa a II-a. De exemplu: pentru populatiile arabe - antigenii DR4 si pentru japonezi DRw6. Diferite asociatii au mai fost facute intre SM si anumiti antigeni determinanti pentru structura imunoglobulinelor G (Ig G) si a receptorilor celulelor T, dar acestea depind foarte mult de fondul genetic individual, rezultand de aici multiple posibilitati de combinare, deci sisteme imune mult diferite de la persoana la persoana.
In cadrul teoriei imunogenetice a bolii trebuie sa se porneasca de la doua criterii de baza :
1. fondul genetic al persoanei
2. dezordinile suferite in cadrul sistemului imun.
Fondul genetic este reprezentet de moleculele de H.L.A. clasa a II-a in special, care creeaza un mediu favorizant aparitiei SM, mai mult decat la alte persoane, in primul rand prin rolul pe care il are procesul de activare leucocitara.
Dezordinile leucocitare reprezinta inceputul activarii celulare a sistemului imunocompetent in sensul unei hiperactivitati a celulelor B limfocitare (demonstrata de prezenta plasmocitelor si cresterii sintezei de IG G in lichidul cefalorahidian (LCR) si SNC precum si distribuirea oligoclonala (manifestata prin cresterea numarului de limfocite T, mai ales purtand receptorii CD4 si CD29).
Problema, care se pune, ar fi puntea de legatura dintre acesti doi factori (fondul genetic si activarea celulara) si care este, de fapt, cheia procesului patogen, din pacate insuficient cunoscut.
Ca si in orice proces autoimun, declansarea actului primordial al bolii poate fi interpretata ca un veritabil arc reflex cu cele 3 componente fundamentale:
1) calea aferenta - antigenul este prezentat de catre HLA celulelor imunocompetente care au receptori specifici pentru fiecare antigen,
2) centrul de prelucrare - procesul complex de descifrare imuno-genetica de la nivelul celulelor imunocompetente,
3) calea eferenta: celulele proliferate spre o anumita linie, corespunzator tipului de antigen, conlucreaza fie pe linie umorala, rezultand anticorpi monoclonali, fie pe linie celulara rezultand celule T citotoxice.
Pentru a putea vorbi cu siguranta despre o eventuala autoimunitate in SM, trebuie clarificat un lucru foarte important si anume posibilitatea migrarii celulelor imunocompetente din sange in sistemul nervos central.
Se stie ca SNC este un timent deosebit prin faptul ca este foarte bine izolat de bariera hematoencefalica (BHE), situata dupa GOLDMANN (1909), la nivelul capilarelor cerebrale.
Doua experimente cumulate au dus la formarea acestui concept:
1) ERLICH a injectat coloranti acizi in vena si singurul organ in care colorantul nu s-a fixat, a fost creierul (interpretarea a fost pusa pe seama lipsei de afinitate a creierului pentru acest colorant).
2) GOLDMANN a facut experienta inversa, a injectat bleu try pan in LCR si a constatat colorarea numai a sistemului nervos; aceste date au dus la formarea conceptului de BHE.
Aceasta este impermeabila in mod normal, pentru o serie de substante care se gasesc in sange, incepand de la proteine - la celulele componente
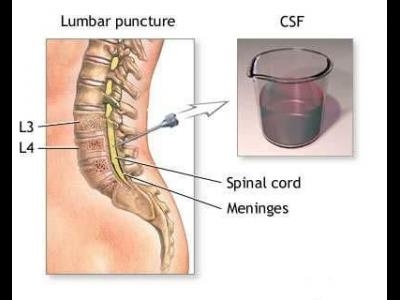
sau chiar medicamente, fapt dovedit de prezenta foarte redusa in mod normal a celulelor sanguine (5 celule/cm3 ) in LCR. Din acestea 90% sunt limfocite.
In cazul inflamarii SNC, bariera hematoencefalica devine permeabila pentru mai multe tipuri de celule (PMN, limfocite). Astfel se poate explica ajungerea in SNC a celulelor imunocompetente.
Nu se cunoaste inca, daca celulele imunocompetente au venit in contact prealabil cu antigenul eliberat in sange,sau daca ele sunt activate local.
Cert este ca prin injectarea in sange de proteina bazica mielinica se poate induce un raspuns asemanator SM, adica o encefalita alergica experimentala (EAE).
Prezenta de anticorpi in LCR poate fi secundara patrunderii limfocitelor B prin BHE, sau sintetizarii la nivel central al imunoglobulinelor. Totusi o crestere in LCR a IgG nu poate fi patognomica pentru SM, pentru ca sunt crescute si in afectiuni de origine infectioasa a SNC, cel mult poate fi folosit ca diagnostic diferential, pentru ca totusi gamaglobulinele sunt prezente in 90% din cazurile de SCLEROZA MULTIPLA.
Faptul ca LT strabat BHE a fost demonstrat de HAFLER (1985) si WIENER (1989) prin prelevari sanguine si recoltari de LCR de la bolnavi cu SM care au fost injectati cu anticorpi antireceptori ai celulelor T (CD2).
In sange s-a observat o crestere de anticorpi anti-CD2 dupa 72 de ore.
In primele 18 ore dupa perfuzie, cresterea numarului LT cu anticorpi anti-CD2 in LCR este evidenta.
Principala concluzie care s-ar putea desprinde de aici este ca, in cazul SM exista intr-adevar o reactie din partea sistemului imun si imuno-supresoarele ar putea stagna procesul progresiv al demielinizarii nervoase a SNC, cel putin catva timp.
Odata ajunse la nivelul SNC, celulele imunocompetente incep sa-si manifeste actiunea contra autoantigenilor, care indreapta actiunea sistemului propriu de aparare impotriva propriei mieline.
Cea mai buna dovada ca in etiologia SM ar putea intra o actiune autoimuna este insusi faptul ca un tratament antiinflamator, si mai ales imunosupresor dau rezultate bune in ceea ce priveste remisia fenomenelor, pe o oarecare durata de timp.
Problema de la care trebuie pornit insa, este cum se activeaza celulele imunocompetente, periferic sau local, care este antigenul ce determina inducerea activarii lor si prin ce efectori se produce demielinizarea? Aflarea acestor probleme ar reprezenta cheia etiologica a SCLEROZA MULTIPLA.
In acest sens o serie de cercetari au efectuat diferite experimente. Lucrarea de fata prezinta datele de laborator si rezultatele obtinute de CHOFFLON si colaboratorii de-a lungul anilor.
Evidentierea proceselor imune in timpul evolutiei SM a fost pusa prin dozarea imunoglobulinelor sau anumitor substante coloidale in LCR. Dozarea imunoglobulinelor a demonstrat, prin imuno-electroforeza, o crestere a gama globulinelor. S-a observat o crestere a IgG mai ales la nivelul LCR, in diferitele procese inflamatorii cerebrale ca: neurosifilisul, dar concentratia lor la acest nivel era mai mare decat in ser. Daca s-ar presupune o rupere (intrerupere) a BHE, atunci cele doua concentratii de IgG ar fi egale. Acest lucru denota ca celulele producatoare de IgG strabat selectiv BHE si prolifereaza la acest nivel.
Din testele de electroforeza (ELFO) in ser, prin migrare la inceput pe agar (TISELIUS 1957) apoi pentru LCR (L WENTHAL ,1960-l964) aratau o distributie oligoclonala a gamaglobulinelor, cu locul de migrare a gamaglobulinelor cu multiple benzi, separate sau nu, ce traduc o productie locala, pentru ca in ser, aceasta distributie nu a fost gasita (sinteza intratecala).
Aproximativ 70% din pacientii bolnavi ai lotului de cercetat au prezentat sinteza intratecala de IgG.
Aceasta crestere a IgG in LCR, chiar daca nu este patognomonica pentru SM (pentru ca s-a dovedit prezenta sa si in infectii cronice ca encefalita luetica, herpetica, PES, neurocisticercoza, sindrom paraneoplazic al SNC), este totusi de valoare paraclinica, dar nu se stie daca sunt practic markeri ai maladiei (pe langa multi altii), sau joaca rol in patogeneza?
Acest aspect oligoclonal pe ELFO, nu se intalneste ca morfologie constant pe ELFO a diferiti pacienti, dar pe parcursul evolutiei bolii la acelasi individ, ea ramane constanta.
GOSWAMI (1987) a gasit in LCR al unui lot restrans de bolnavi de SM, anticorpi contra structurii paramixovirusilor (anticorpi anti-SV5) in 55% din acestia. PERRON si colaboratorii (1989) au izolat un retrovirus (LM7-necunoscut pana atunci) in leptomeningele unor bolnavi de SCLEROZA MULTIPLA. Prezenta acestui anticorp in LCR, la unele persoane cu SM, dar si a unui numar considerabil de persoane sanatoase, nu poate fi considerata semnificativa. Totusi, ramane in continuare un semn de intrebare pentru teoria mixta (autoimuno-infectioasa).
De asemenea, tot in LCR s-au descoperit lanturi usoare k si lambda ale IgG, care nu sunt produsi de degradarea IgG, ce proteine eliberate de plasmocite (in 80% din cazuri).
Determinari asemanatoare cu cele in LCR au fost facute in lacrimi, datorita diferentei de compozitie a lor fata de ser.
Prezenta acestor anticorpi in LCR nu se poare explica prin patrunderea libera a lor (care sunt proteine) prin BHE, ce implica o difuzie selectiva, in primul rand a celulelor B, care apoi vor prolifera imunoblastic. Aceasta proliferare ar putea fi indusa de niste factori stimulatori eliberati de limfocitele T. Se va vedea mai tarziu care este subpopulatia limfocitelor T, descoperita in LCR al bolnavilor de SCLEROZA MULTIPLA.
In ceea ce priveste limfocitele T, se clasifica in limfocite natural killer, limfocite killer, si limfocite T helper. Limfocitele natural killer nu necesita in prealabil un contact cu agentul si pot distruge celule non-self.
Pentru o cunoastere mai buna a semnelor clinice ale SM, s-a incercat obtinerea experimentala, cel putin al unor forme asemanatoare, care dau modificari anatomice apropiate.
Experimentele au fost efectuate pe cobai, caini etc, folosind ca antigen mielina si adjuvantul lui Freud, proteina bazica mielinica (PBM).
Stimularea celulelor T presupune preexistenta pe suprafata lor a unor receptori care pot prelua informatia de la prezentatorii de antigen.
Drumul de stimulare se poate face prin receptorii CD3/TCR sau CD2.
Un factor de stimulare este molecula de histocompatibilitate clasa a II-a.
Unele din cele mai importante mitogene, care stimuleaza LT specific sunt: fitohemoglutinina (PHA), concaralina A (con A), anticorpi monoclonali legand complexul CD3/TCR sau antigena de diferentiere CD2, forbol mystrat-acetat (PMA), asociat cu ionomicina sau interleukina 2.
Observatia principala pe care au facut-o CHOFFLON si colaboratorii, a fost o diminuare a activitatii celulelor mononucleate in LCR, ativ cu cele sangvine, dar acest lucru a fost intalnit atat in cazul bolnavilor de SM, cat si la bolnavi cu alte boli inflamatorii ale SNC.
O ipoteza ar fi fost un numar insuficient de celule prezentatoare de antigen, adica de macrofage. Dar CHOFFLON si colaboratorii au introdus in LCR, printr-o tehnica clasica de aderenta la plastic, celule macrofage, si dupa marirea numarului lor, celulele T au fost insuficient proliferate specific. Ceea ce dovedeste existenta unui alt tip de mecaniSCLEROZA MULTIPLA.
Ceea ce face dificila explicarea oricarui mecanism de activare in SM este faptul ca aceasta boala evolueaza in pusee. Un prim puseu este urmat de altele, cu agravare din ce in ce mai pronuntata a fenomenelor clinice neurologice.
Din punct de vedere neurologic ne punem problema eventualitatii unei reactii celulare.
Aceasa idee presupune existenta unui mesaj informational reluat intr-un anumit mod, la un anumit contact cu un antigen.
O interesanta concluzie a experimentului condus de CHOFFLON si colaboratorii, a fost prezenta in LCR, predominant a celulelor citotoxice,
helper-inducer care ar distruge tesutul nervos si o cantitate foarte mica de celule suppressor-inducer, celule ce ar stopa efectele distructive.
Acest fapt a fost pus in evidenta prin prezenta in LCR de celule predominante, avand pe suprafata lor moleculele: CD4+CDw29+ si foarte putine celule de suprafata CD4+CD45 RA+.
Stimularea acestor doua tipuri de celule a fost obtinuta pe culturi de celule cu anti-CD2 si PMA.
Prin administrarea acestor anticorpi anti-CD2 la bolnavi cu SM s-a obtinut o slaba proliferare de celule CD4+CDw29+ pentru ca sunt slab reprezentate in LCR.
In schimb, administrarea lor la bolnavi cu maladii inflamatorii ale SNC, este urmata de o proliferare considerabila a celulelor suppressor-inducer.
Scaderea numarului acestor celule se realizeaza atat in sange cat si in LCR.
Se pare ca un rol important in patrunderea celulelor T CD4+CDw29 a fost explicata prin studiul structurii moleculei CDw29+ care ar putea trece selectiv BHE.
Asociindu-se celulelor prezentatoare de antigeni, aceasta molecula ar favoriza adeziunea celulei la endoteliul capilar si ar da o informatie mai buna asupra functiei sale de helper-inducer.
Celula T activata este recunoscuta dupa o molecula de antigen situata pe suprafata ei, numita Ta1 care nu se afla pe celulele neactivate. Aceasta molecula a fost descoperita pe suprafata celulelor T din LCR, al bolnavilor de artrita reumatoida si SCLEROZA MULTIPLA.
Celulele T activate, care prezinta pe suprafata lor aceasta molecula, se presupune ca sunt celule cu memorie, cu posibilitatea reactivarii actiunilor lor in cazul reintalnirii lor cu acelasi antigen.
CHOFFLON si colaboratorii au efectuat reactia autologa limfocitara mixta (AMLR), care masoara puterea supresiva a celulelor, pe un lot de 13 oameni sanatosi si 6 bolnavi de SM, efectuand culturi de celule sangvine nucleate care au fost puse in contact cu celulele producatoare de IgG stimulate prin poke weed mitogen (PWM). Puterea supresiva a fost exprimata procentual prin formula:
% supresie = Ig G(MNC+PWM) - Ig G(MNC+PWN+Tcells post AMLR) 100
unde:
- Ig G(MNC+PWM) concentratia de Ig G (mg/ml) in cultura de celule mononucleate (MNC) ale donatorului alogenic stimulate cu poke weed mitogen (PWM) - acelasi donator pentru tot studiul.
Ig G(MNC+PWM+Tcells post AMLR)=concentratia Ig
G (mg/ml)
din cultura de celule mononucleate ale donatorului alogenic, PWM si celule
T post AMPR, a carei activitati supresive vrem s-o masuram.
In urma acestei reactii, s-a constatat o diminuare a activitatii supresive a celulelor recoltate din LCR al bolnavilor cu SCLEROZA MULTIPLA. Care ar fi efectorii acestui proces ? Pana acum, doar teoretic, se considera 3 substante: 1) factorul de necroza tumorala alfa (FNT alfa), 2) interleukinele (IL) si interferonul gamma (ITF gamma).
Se stie ca celulele agresate infectios, determina formarea de celule activate ce secreta asa numitele citokine. In aceasta categorie intra si cele trei substante enumerate mai sus. Aceste citokine sunt importante mediatoare de inflamatie si capabile sa modifice proprietatile celulelor endoteliale.
FNT alfa produs de astrocite si de celulele microgliei are puternice efecte asupra celulelor SNC, fiind toxic pentru mielina si oligodendrocitele producatoare de mielina. Acest factor poate actiona in sinergie cu interferonul gamma asupra moleculelor CMH clasa I-a si a II-a, care au si ele rolul lor in demielinizare.
In raport cu diferitele faze ale bolii (puseu acut sau remisie), pe lotul experimental al lui CHOFFLON s-au obtinut urmatoarele date in ceea ce priveste concentratia de citokine in ser (FNT alfa):
VN=143+25 pg/ml - (la sanatosi)
721 +/- 58 pg/ml - la cei in remisie (forma cronica progresiva) a SCLEROZA MULTIPLA.
In LCR s-a determinat o crestere discreta a FNT alfa in puseul acut al SM si o crestere foarte marcata a FNT alfa in forma cronica progresiva.
Prelevari ulterioare de sange si LCR de la 34 bolnavi cu SM, din care 33 au luat ca tratament unic prednison si unul singur ciclofosfamida, au evidentiat urmatoarele:
din cei 33 de pacienti urmariti bilunar, 17 au prezentat 7 pusee, dupa intreruperea tratamentului, de fiecare data aceste pusee fiind precedate la 2-4 saptamani de cresteri importante a FNT alfa.
la pacientul ce luase ciclofosfamida, pe o perioada de 5 luni, concentratia de FNT a fost constanta. A precedat puseul o crestere a FNT, concentratia mentinandu-se crescuta, pana la reluarea tratamentului imunosupresor.
FNT alfa si FNT gamma au fost vazute deci ca citokine capabile sa declanseze un nou puseu. In sprijinul acestei idei a venit si observatia ca in timpul unui stress sau infectii virale, se agraveaza simptomele bolii, tocmai prin aceasta hiperproductie de ITF gamma.
Ce ne determina si mai mult sa consideram ca SM este o boala autoimuna ?
Faptul ca aceasta boala este legata direct de o dezordine imunologica, asociata sau nu cu factori ereditari sau de mediu, faptul ca modelul experimental al SM, encefalita alergica experimentala (EAE), se poate obtine prin transferul de celule T sensibilizate la PBM, de la un animal bolnav la unul sanatos (10.000 de celule injectate subcutan sunt suficiente), faptul ca PBM actioneaza ca o autoantigena, evidentierea clara a trecerii BHE de catre celulele activate periferic, formarea complexului trimolecular (receptor al celulelor T/TCR+moleculele de histocompatibilitate MHC clasa a II-a+antigenul) si prezenta de celule citotoxice de tip help-inducer cu evidentierea de citokine crescute in ser si LCR - acestea sunt elemente concrete ce ne pun in legatura cu eventualitatea autoimuna a bolii.
In ultimii ani, o serie de ercetari au avut ca scop evidentierea unor noi antigene, ca si peptidele sintetice din secventa PBM umane, PMB+adjuvantul lui Freud, proteolipide (PLP).
In 1990, OTA si colaboratorii, au pornit un experiment care avea ca si concluzie evidentierea unor celule specifice ce raspund la PBM. Faptul a fost demonstrat mai ales pentru fragmentul encefalitogen 84-l02 al PBM asociat cu frecventa crescuta a DR2 si pentru fragmentul 143-l68 asociat cu DRw11.
Deci cel mai bun antigen pentru evidentierea modelului experimental al SM, a fost PBM.
Tot in sprijinul clasarii SM drept maladie autoimuna, vin asocierile, discrete, ce este drept, acestei boli cu altele, deja recunoscute ca auto-distructive: poliartrita reumatoida, tiroidita Hashimoto, lupusul eritematos diseminat, miastenia gravis, pemusul bulos.
Cunoasterea diferitelor mecanisme din aproape in aproape, urmarind ipotetic anumite reactii si efecte posibile manifestate de diferite antigene, s-ar putea ca intr-un viitor apropiat sa putem actiona cu eficienta asupra acestei boli, nu numai sa ii incetinim evolutia.
Cea mai importanta etapa a procesului imun este self-toleranta prin care s-ar parea ca autoantigenele, venind in contact cu macrofagul si limfocitul in complex trimolecular, proces ce se desfasoara in timus, ar determina distrugerea acestui complex de niste mecanisme foarte bine stabilite.
S-a conturat astfel ideea unui tratament per os de autoantigene care ajung in sange, sensibilizeaza aceste mecanisme distructive ale auto-complexului trimolecular si dau o stopare a initierii procesului autoimun. In acest sens s-a actionat nu numai in directia tratarii SM, dar si a altor maladii autoimune.
Astfel, din 1993 WEINER si colaboratorii a determinat un grup de bolnavi de SM sa ia zilnic o doza de PBM bovina orala, avand ca prime rezultate incetinirea evolutiei bolii. Administrarea de antigena S, pe cale orala a suprimat uveita experimentala, iar administrarea orala de colagen II, surprima artrita experimentala, indusa de colagen si adjuvantul lui Freud (THOMSON si colaboratorii, 1986; NAGLER, ANDERSON si colaboratorii 1986, ZANG si colaboratorii 1990).
Tratamentele eficiente vor trebui astfel sa atinga toate treptele evolutiei autoimune: BHE, complexul trimolecular, self-toleranta, posibilitatea inducerii supresiei, iar ca obiective mai indepartate - remielinizarea, regenerarea axonala si de ce nu, o eventuala regenerare neuronala.
Se considera ca SM este rezultatul unei interactiuni complexe intre factorii declansatori de mediu (cum ar fi infectiile), predispozitia genetica si activarea aberanta a celulelor sistemului imun (ALOTAIBI S., 2004).
Studiile epidemiologice sugereaza ca expunerea ambientala la un anumit agent infectios trebuie sa se produca intr-o fereastra de vulnerabilitate imunologica specifica varstei copilariei (ASCHERIO A. si colab., 2000).
Virusul Epstein-Barr (V.E.B.) prezinta un interes particular. Infectia acuta simptomatica cu VEB (mononucleoza infectioasa) se poate asocia cu demielinizari la nivelul sistemului nervos central (BRAY P.F. si colab. 1992). Desi majoritatea pacientilor adulti cu SM nu au semne clinice sau serologice de mononucleoza acuta, in momentul stabilirii diagnosticului de SM, aproape toti prezinta markeri serologici de infectie veche cu VEB (LARSEN P.D. si colab. 1985; BRAY P.F. si colab. 1983). Chiar daca asocierea dintre infectia cu VEB si SM la adult este semnificativa statistic, relevanta etiopatogenica a acestei observatii a fost pusa la indoiala, cata vreme VEB este prezenta la mai mult de 90% dintre populatia adulta sanatoasa din societatile occidentale (ASCHEIRO A. si colab., 2001).
Infectia cu VEB survine in copilarie sau in adolescenta la 50% dintre indivizi (EVANS A.S. si colab. 1989), ceilalti contracteaza virusul in perioada de adult tanar. La aproximativ 5% din totalul pacientilor cu SM, boala debuteaza inaintea varstei de 18 ani (DUQUETTE P. si colab., 1987; GHEZZI A. si colab., 1997).
Daca infectia cu VEB este intr-adevar implicata in declansarea SM, atunci copin cu SM trebuie sa aiba do serologice ale expunerii anterioare la VEB, in momentul stabilirii diagnosticului de SM, la o varsta la care nu au fost inca expusi la virus.
Un studiu privind relatia dintre virusul VEB si SM a fost realizat pe 35 copii cu diagnosticul cert de SM (dupa criteriile lui POSER C.M.1983) aflati in evidenta Clinicii de Neurologie Pediatrica a Spitalului de Pediatrie din Toronto, Canada in februarie 2003 (ALOTAIBI G., 2004). Selectia lotului martor s-a bazat pe disponibilitatea rezultatelor serologice pentru VEB sau a probelor de ser conservat in cadrul departamentului de virusologie. Pentru studiul copiilor sanatosi s-au ales probe obtinute de la donatorii de maduva osoasa pentru transt (TMO). Pentru a rezolva corespondenta de varsta s-au selectat probe de la o serie de pacienti care se prezentasera la departamentul de urgenta (DU), raportul martori de aceeasi varsta (pacienti cu SM fiind de 3/1).
Infectia veche de VEB a fost descoperita la 83% dintre pacientii cu SM, fata de 42% dintre martorii TMO si 42% dintre martorii sanatosi cu varste similare din lotul DU.
Doar 17% dintre pacientii cu SM au fost seronegativi pentru VEB, fata de 55% in grupul donatorilor TMO si respectiv 36% dintre subiectii control din DU. Dupa cum reiese, cea mai mare rata a infectiilor recente s-au inregistrat in lotul DU (22%), in care testele serologice au fost efectuate tocmai datorita suspiciunii clinice de infectie acuta cu VEB. La copin cu SM nu s-au descoperit do de infectie recenta cu VEB, nici chiar la cei la care proba de sange a fost prelevata in momentul primului episod demielinizant. Intre pacientii cu SM si martori nu s-au inregistrat diferente in ceea ce priveste prevalenta anticorpilor impotriva paravirusului B19, dar probabilitatea expunerii la VHS a fost mai mica la copin cu SM decat la subiectii control.
Copin cu SM au probabilitatea semnificativ mai mare de a fi infectati cu VEB, decat subiectii sanatosi de aceeasi varsta. Rezultatele pot fi interpretate in mai multe moduri:
1. Infectia cu VEB initiaza sau intretine patogeneza SM;
2. SM in sine creste susceptabilitatea limfocitelor B de a fi infectat cu VEB;
3. Exista un mecanism comun ce determina cresterea susceptibilitatii la infectia precoce cu VEB si la SM cu debut precoce.
In patogeneza SM poate fi implicat raspunsul imun la diversi factori de mediu, cum ar fi virusii cu care copin vin in contact in fereastra de risc specifica acestei varste (MARTYN C.N. si colab., 1993; POSKANZER D.C, 1980; MARRIE RA. si colab., 2000; HAAHR S. si colab., 1997).
O serie de caracteristici ale VEB fac posibila, din punct de vedere biologic, ipoteza conform careia acest virus ar putea juca un rol in patogeneza SCLEROZA MULTIPLA. Expunerea la VEB are ca rezultat infectia persistenta a limfocitelor B, prolifererea clonelor de celule B transformate viral si sinteza de anticorpi indreptati impotriva anumitor antigene virale; totodata celulele B infectate se afla sub supraveghere continua a limfocitelor T (BRAY P.F. 1992). Prezenta limfocitelor T raspunzatoare la stimulul antigenic reprezentat de VEB nu are in mod inerent semnificatia patologica, intrucat aceste celule sunt prezente in stare latenta la majoritatea adultilor sanatosi VEB - pozitivi.
Potentialul patogen al limfocitelor T necesita activarea acestora, posibil prin mimetism molecular. O secventa pentapeptidica descoperita in structura antigenului viral nuclear prezinta similitudini cu un epitop al proteinei bazice mielinice, o componenta majora a tecii de mielina. Mai mult, VEB induce expresia pe suprafata limfocitelor B si alfa - B cristalin, o proteina identificata recent drept un constituient autoantigenic major, a carei expresie este modificata in sistemul nervos central al pacientilor cu SM (VAN NOORT J.M. si colab., 2000). Prin urmare putem presupune ca expunerea la VEB poate induce un raspuns imun gresit directionat al gazdei impotriva propriilor antigene din sistemul nervos central, precum, alfa - B cristalin sau proteina bazica mielinica.
VEB nu este singurul agent infectios implicat in patogenia SM si in mod sigur nu este un factor declansator obligatoriu, dovada cei 5 copii cu SM, VEB-negativi. Posibilul rol al virusului herpetic uman 6 (VHU-6) a fost sugerat de expresia acestui virus la nivelul celulelor sistemului nervos central, ca si de titrurile crescute de anticorpi anti VHU-6 in serul pacientilor cu SM (KNOX K.K. si colab., 2000). Infectia cu virusul herpetic uman 6, varianta A duce la activarea genomului VEB in limfocitele B infectate (CUOMO L. si colab. 1995), avansand posibilitatea actiunii concertate a mai multor virusi. Totusi, datele din literatura referitoare la VHU - 6 sunt dificil de interpretat, din cauza diferentelor metodologice dintre studii (SWANBORG R.H. si colab. 2003) si faptului ca aproape 100% din populatie este deja infectata cu VHU - 6 inainte de a implini varsta de 2 ani. De mai mare interes ar fi evaluarea status-ului replicativ (latent al VHU-6), ce presupune metode moleculare precum tehnicile de amplificare genetica (ALLEN U.D. si colab., 2001). Pe viitor se preconizeaza efectuarea unor astfel de teste. Desi numerosi agenti virali, altii decat VEB (inclusiv Chlamydia pneumoniee) au fost studiati din punct de vedere al posibilului rol patogenic in SM, nu se dispune inca de date certe in formarea anumitor asocieri, fapt datorat, cel putin in parte, diferentelor dintre studii, in ceea ce priveste metodologia si pacientii inclusi (GRANIERI E. si colab., 1997). Este posibil ca asocierea dintre infectia cu VEB si SM sa fie legata de intensitatea expunerii la virus sau de susceptibilitatea crescuta la infectia cu VEB a copiilor cu SM, mai degraba decat sa reflecte o legatura de tip cauza efect. Totusi, copin cu SM nu par sa fie mai susceptibili sau mai expusi la infectii virale in general, fapt demonstrat de ratele similare de seropozitivitate pentru parvovirusul B19, CMV si VVZ inregistrate la pacientii cu SM, respectiv la subiectii control.
O alta intrebare importanta este daca infectia cu VEB initiaza, mai degraba decat intretine, procesele imunologice implicate in SCLEROZA MULTIPLA. Un studiu asupra infectiei cu VEB efectuat pe 3 milioane de cadre militare din armata SUA a evidentiat o asociere pozitiva puternica intre prezenta anticorpilor anti-VEB si riscul de SM, probele de sange analizate fiind prelevate cu mai mult de 5 ani inaintea diagnosticului cu SM (LEVIN L. J. si colab., 2003). Mai multe do in favoarea rolului VEB in initierea patogenezei SM pot fi obtinute prin analiza serologiei VEB la copin ce se prezinta cu un puseu acut initial de demielinizare la nivelul sistemului nervos central: copin diagnosticati ulterior cu SM vor prezenta do serologice de infectie veche cu VEB chiar in momentul primului puseu de boala.
O observatie interesanta a studiului intreprins de ALOTAIBI S. si colab. 2004, este faptul ca probabilitatea copiilor sanatosi de a fi seropozitivi pentru VHS este mai mare decat a celor cu SCLEROZA MULTIPLA. Desi metoda de laborator folosita in studiul amintit nu permite diferentiere intre VHS-l si VHS-2, majoritatea participantilor la studiu aveau varste sub 16 ani, prin urmare este putin probabil sa fi fost activi sexual. Astfel, rezultatele serologice ale acestora reflecta cel mai probabil infectia anterioara cu VHS-l. S-a emis ipoteza ca imunitatea fata de VHS-l are efect protector impotriva SM (MARTIN J.R., 1981). Daca secventa expunerilor virale in copilarie este importanta pentru fiziopatologia SM, atunci este posibil ca pacientii pediatrici cu SM sa fi contactat infectia cu VEB fara a beneficia de protectia conferita de infectia anterioara cu VHS-l. Desi datele demografice ale subiectilor din grupurile martor sunt limitate, este putin probabil ca diferentele demografice dintre martori si pacientii cu SM sa fie responsabile de diferentele marcate, in ceea ce priveste rezultatele serologice pozitive pentru VEB. De fapt, caracteristicile demografice ale celor 2 grupuri martor nu au fost selectate in asa fel incat sa fie similare, si totusi seroprevalenta VEB a fost identica. Mai mult, seroprevalenta VEB in randul martorilor a fost similara cu cea raportata in alte grupuri martor pediatrice, dintr-o serie de studii nord-americane asupra infectiei cu VEB (JAMES S. A. si colab., 1997).
In plus, desi esantionul studiat a avut un numar limitat de subiecti, rezultatele obtinute au fost semnificative. Validarea acestor rezultate necesita un studiu mai amplu, de tip prospectiv, cu care sa se analizeze incidenta mai multor agenti virali la copii sanatosi, respectiv cu SCLEROZA MULTIPLA.
Etiologia infectioasa a fost presupusa, datorita studiilor epidemiologie, dar si datorita similitudinilor cu bolile infectioase demielinizante. Totusi, se pare ca agentii infectiosi formuleaza mai degraba raspunsul imun impotriva antigenelor self si pot induce boala doar in anumite circumstante, decat sa poata fi demonstrata implicarea unui singur microb patogen.
Exista studii, care au stabilit conexiuni intre infectiile virale si exarcerbarile din SM, iar studiile migratiilor au demonstrat posibilitatea implicarii unor agenti infectiosi. Bolile demielinizante virale ofera exemple despre cum ar putea infectia virala sa produca demielinizarea. PRATT E. si MARTIN R. (2002) sustin ca demielinizarea este produsa printr-o infectie virala si afectarea directa a oligodendrocitelor. Analize recente neuro-patologice ale leziunilor din SM (LUCCHINETTI C. si colab., 2000) au aratat ca patternul de demielinizare, care se contureaza pare a fi indus initial prin perturbarea oligodendrocitelor. Autorii emit ipoteza ca acesta ar fi rezultatul unei infectii cu un virus necunoscut, sau o afectare mediata de o toxina necunoscuta si ea. Alte boli infectioase, in care se produce demielinizarea sunt: panencefalita sclerozanta subacuta, in care oligodendrocitele infectate viral sunt tinta afectarilor mediate imun, encefalomielita demielinizanta postinfectioasa, in care demielinizarea este mai degraba produsa de un raspuns imun impotriva mielinei, indus de virusurile rujeolei, varicelei, vaccinal. In SM a fost depistat in oligoden-drocitele din maduva spinarii un virus asemanator paraparezei spastice tropicale, boala care mimeaza SCLEROZA MULTIPLA. Dintre factorii microbieni, studii recente au raportat o asociere a Chlamydiei pneumonie cu SCLEROZA MULTIPLA. O alta varianta este cea in care agentii infectiosi pot declansa un raspuns autoimun prin infectarea tesuturilor tinta (de ex. oligodendrocitele), pe calea mimetismului molecular (PRATT E. si MARTIN R., 2002).
Se observa ca etiologia SM este multifactoriala, aflata la intersectia interactiunilor dintre factorii de mediu cu factorii genetici (OKSENBERG J. R. si colab., 2000) care confera susceptabilitate la boala sau modifica evolutia acesteia, ducand la o expresie heterogenica, care priveste aspectele clinice, histopatologice si genetice. (LUCCHINETTI C. si colab., 2000; BARCELLOS L.F. si colab., 2001).
In acest moment, singura asociere certa intre factorii genetici si susceptibilitatea la SM, este dovedita la nivelul haplotipului HLA DR2 pentru alelele DR B 1501, Dr B10101 si DQB1 0602, DQA1 0102, din genele CMH situate pe cromozomul 6. Aceasta asociere a fost demonstrata atat prin linkaj, cat si prin asociere in studii familiale si caz-control, dar mecanismul exact prin care aceasta asociere determina suscetibilitatea la boala nu este pe deplin cunoscut. Totusi, se pare ca genele MHC HLA DR B1 1501 si HLA DR B1 0602 pot codifica moleculele de recunoastere clasa II, cu o predilectie pentru legarea antigenelor peptidice ale mielinei si stimuleaza celulele T encefalitogene; HLA DR alfa 0101- DR beta 1501 heteromer, care leaga cu mare afinitate MBP in regiunea reziduurilor peptidice 58-99.
Cristalografia cu raze X a complexului peptidic DR-MBP releva o structura moleculara diferita a DR beta 1501 fata de DRa, in ceea ce priveste reziduurile aril, care prefera buzunarul P4 al domeniului de legare a proteinei (GAUTHIER L. si colab., 1998; SMITH K. J. si colab., 1998). In plus, pe cele doua fete ale laturilor peptidice ale portiunii P85-99 M.B.P., care apartine peptidului imunodominant, au fost gasite Val. 89 si Phe 92, ca fiind ancorele principale si aceasta explica marea afinitate de legare a MBP la HLA-DR alfa 0101/DR beta 1501. Analiza structurala releva si faptul ca doar 2 reziduuri de contact primar cu TCR ale MBP p85-99 au fost conservate, pentru a stimula in mod adecvat clonele de celule Ag - specifice (HAUSMAN S. si colab., 1999). Aceasta sugereaza ca peptidele microbiene, care prezinta doar o secventa limitata identica cu cea a unei peptide proprii, pot activa celulele T autoreactive.
Ca un corolar al celor prezentate mai sus, s-a demonstrat ca locusul MHC prezinta si asociere si linkaj cu SM in studii caz-control si familiale. Totusi, rolul unei gene din acea regiune, in determinarea caracteristicilor clinice sau subtipurilor de SM este inca neclar. Cu toate acestea a fost raportata o asociere a HLA-DR2 cu un debut precoce, sever de tip recurent-remisiva si cu o evolutie mai blanda a SCLEROZA MULTIPLA.
In modelul EAE, genele MHC par a influenta in primul rand susceptibilitatea si penetranta, in timp ce alti loci moduleaza specific fenotipul, cum ar fi localizarea in creier sau maduva spinarii, demielinizarea si severitatea inflamatiei. Prin analogie ar fi de interes identificarea locusurilor implicate in evenimentele patogene initiale ale bolii sau a celor ce influenteaza dezvoltarea acesteia. Aici sunt de luat in consideratie genele, care - din punct de vedere logic - au posibilitatea sa joace un rol in evolutia bolii, acestea fiind denumite gene candidat. Pentru SM, acest tip de gene sunt cele reprezentate de cele care pot codifica citokinele, receptorii imunologici, componentele mielinice si proteine implicate in clearence-ul viral (Multiple Sclerosis Genetics group California at San Francisco, 2002).
Cateva studii examineaza influenta unui astfel de grup de gene, cum ar fi 1L-lR (care a fost asociat cu o forma de boala mai severa, care progreseaza mai rapid COYLE P. K., 2000) , TNF, Ap0E, CTLA4 si CCR5, asupra cursului si severitatii SM si asteapta si alte confirmari.
Dupa HUFSCHMIDT S. si L CKING G. H. (2002) rudele de gradul I au un risc de imbolnavire crescut de 15-25 ori.
  |
  |
  |
  |
Ce este ateroscleroza si ce consecinte are. Ateroscleroza inseamna infiltrarea peretilor arterelor cu grasimi, dintre care colesterolul este dom [...] |
Aceasta boala este asociata de obicei cu hipertensiunea arteriala. in ateroscleroza, se produce o infiltrare a stratului intim al arterelor, dar si su [...] |
La originea bolii figureaza o alimentatie bogata in grasimi de origine animala, un mod de viata stresant (incordare nervoasa, necazuri etc), [...] |
Copyright © 2010 - 2025
: eSanatos.com - Reproducerea, chiar si partiala, a materialelor de pe acest site este interzisa!
Informatiile medicale au scop informativ si educational. Ele nu pot inlocui consultul medicului si nici diagnosticul stabilit in urma investigatiilor si analizelor medicale la un medic specialist.
Termeni si conditii - Confidentialitatea datelor - Contact