|
|
1. Introducere
De la data diagnosticarii primului caz de trichineloza la om (1868) si pana astazi, s-au acumulat numeroase date privind ciclul biologic al agentului parazitar, caile de transmitere, receptivitatea, mijloacele terapeutice si de profilaxie, alaturi de mecanismele patogenice cu particularitatile imunologice ale acestei afectiuni larg raspandita in tarile unde se consuma carne de porc, cal, mistret sau urs.
Datele statistice demonstreaza ca in perioada 1963-l968 media anuala a cazurilor de trichineloza era de 79,7, iar in perioada 1969-l986 de 250-400. In anii care au urmat, extensia cazuisticii a crescut neincetat. In 1987 se ajunge la 538 cazuri, in 1988 la 825 cazuri, iar in 1989 la 947 cazuri. Incepand cu 1990, media anuala a numarului de cazuri depaseste 1000 si in urmatorii ani creste de peste 3,5 ori. In intervalul 1982 1999 s au inregistrat 20.296 imbolnaviri umane de trichineloza, din care peste 80% au aparut in perioada 1990-l999.
La animale este o certitudine faptul ca parazitarea a crescut. Daca in 1992 s-au diagnosticat la porcine, trichineloscopic, 6892 cazuri, in 1993 au fost 10.540 cazuri pozitive, reprezentand cel mai mare numar de porci cu trichineloza inregistrat vreodata in Romania. Trebuie mentionat ca, cel putin jumatate din porcii parazitati prezentau infestatii masive, deci un potential trichinelogen considerabil si deosebit de periculos, care a fost eliminat din consumul uman.
In ultimele doua decenii, cabalinele au intrat in categoria animalelor care, nu numai ca sunt foarte receptive la invazia cu Trichinella, dar prezinta si pericol epidemio epizootologic real. In tarile Comunitatii Europene se acorda o atentie deosebita nu atat trichinelozei la porcine, care poate fi controlata eficient, cat invaziei la cabaline si deci, posibilitatilor reale de infestare a populatiei umane, prin consumul carnii si produselor din carne de cal.
Incepand cu 1975, sursa majora a trichinelozei la om, in Italia, a constituit-o carnea provenita de la caii importati din Europa de Est. Din aceasta cauza, toate loturile de cai provenite din Europa de Est sunt supuse trichineloscopiei si digestiei artificiale pentru Trichinella. Situatia trichinelozei la cabaline este similara in Franta si Spania. Situatia se reflecta in Romania prin prisma relatiilor comerciale cu aceste tari.
Incidenta la animalele salbatice (trichineloza silvatica) este foarte dificil de estimat. Importanta practica ce poate fi retinuta, ca pericol pentru infectarea omului si a altor mamifere, o reprezinta doar mistretii si ursii, a caror carne este comestibila.
In anul 1835, un tanar student la Medicina din Londra, James et, in timp ce studia anatomia pe un cadavru de om, a descoperit in musculatura acestuia o sumedenie de chisturi foarte mici. In interiorul acestor misterioase formatiuni erau niste viermisori incolaciti, vizibili doar la microscop, pe care un savant zoolog, Richard Owen din Londra, i-a denumit Trichina spiralis, pentru ca se asemanau cu firisoare de par trichus rasucite sau spiralate. Mai tarziu, in 1895, un savant francez Railliet, pentru a evita confuzia cu numele unor insecte, le-a schimbat denumirea din Trichina spiralis in Trichinella spiralis, termen ramas valabil pana in zilele noastre. Ulterior, Trichinella spiralis a fost identificata si in alte cadavre umane, precum si in carnea de porc, caini, pisici, sobolani si alte specii de animale.
In 1860, o fata din Dresda (Germania), consumand carne de porc infestata, s‑a imbolnavit grav si a decedat. La necropsia cadavrului, medicul german Zenker, a gasit un numar considerabil de parazti adulti in intestin si larve in musculatura. Carnea, din care a consumat tanara decedata, era masiv infestata cu larve de Trichinella spiralis. Cu tesut muscular din cadavru, a fost infestat un caine, iar cu forme adulte, recoltate din intestinul acestuia, infestatia a fost transmisa la porc si de la porc, la iepure. Astfel, s-a dovedit ca Trichinella spiralis poate infecta atat omul, cat si diferite specii de animale.
In 1862, a fost precizat diagnosticul bolii la omul in viata, dupa semnele clinice, diagnostic confirmat prin biopsie. Boala a fost denumita, la inceput, trichiniasis sau trichinoza si mai tarziu, trichineloza, denumire folosita si in prezent.
In Romania, primul caz de trichineloza a fost depistat in 1868 de dr. Scheiber, la necropsia unui cadavru de la spitalul Coltea din Bucuresti, iar la sfarsitul aceluiasi an, in urma unor masuri organizatorice, a fost descoperit prin examen microscopic si primul porc cu trichine, dovedindu-se astfel, existenta trichinelozei la porcii crescuti pe teritoriul tarii noastre. In 1869, s-a realizat prima infestare experimentala cu probe de muschi parazitat de la om, la porc, caine si pisica si modelarea experimentala prin administrare in hrana animalelor.
In 1913, s-a legiferat obligativitatea controlului trichineloscopic al tuturor porcinelor taiate in abatoare. Masura, luata cu 81 de ani in urma, s-a dovedit, asa cum o atesta proba timpului, de o exceptionala importanta, avand implicatii ce s-au valorificat consistent in protectia sanitara a populatiei umane.
Trichinella spiralis, agentul etiologic al trichinelozei, face parte din genul Trichinella, familia Trichinellidae, clasa Nematode.
Trichinella spiralis este un parazit unisexuat, care are corpul acoperit de o cuticula chitinoasa si transparenta.

. 1. Trichinella spiralis, femela adult
Femela masoara intre 34 mm, iar masculul aproximativ 1,5 mm. Catre extremitatea anterioara a adultilor, c 414b15e orpul acestora se ingusteaza. Tubul digestiv prezinta un esofag lung si subtire care, dupa strapungerea inelului nervos, capata forma unui bulb. La capatul extremitatii posterioare a nematodului, tubul digestiv se deschide prin orificiul anal.
Din punct de vedere anatomic, femela prezinta un ovar, oviduct si un uter, care se continua cu vaginul. Acesta se deschide la nivelul 1/5 extremitatii ventrale a parazitului.

. 2. Trichinella spiralis, mascul adult
Masculul prezinta o extremitate anterioara subtire, prevazuta cu un aparat bucal minuscul, un tub digestiv lung si subtire si o extremitate posterioara incurbata, unde se afla doua excrescente mici conice. Nu prezinta spicul, dar detine un canal deferent aflat in continuarea testiculului, canal care se exteriorizeaza in zona terminala a intestinului.
Larvele tinere masoara 80120 microni lungime si 56 microni latime. Au corpul acoperit de o cuticula subtire, fin inelata. Ajunse in muschi, cresc pana la dimensiunea de 8001000 microni, se incolacesc, se izoleaza intr-un chist si devin infectante. Chistul are forma ovalara, cu axa mare indreptata in directia fibrelor musculare si masoara intre 300‑800 microni lungime si 200400 microni latime. De regula, in interiorul fiecarui chist se afla o singura larva.
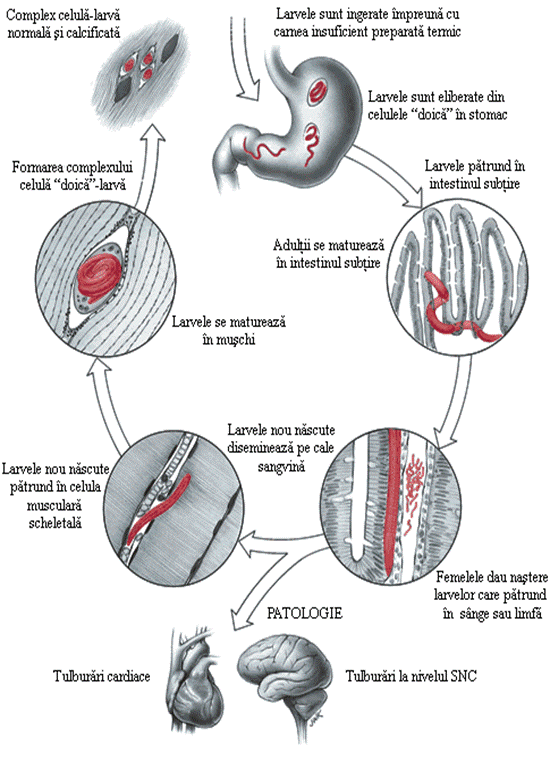
. 3. Ciclul biologic
Ciclul biologic este caracteristic si anume autoheteroxen, in sensul ca aceeasi persoana, este la inceput gazda definitiva, iar ulterior devine si gazda intermediara.
Parazitul este introdus in tractul digestiv uman sub forma de larva inchistata in muschii unor animale. Sub actiunea enzimelor digestive ale stomacului, larvele sunt eliberate din chistul muscular. Dupa ce au ajuns in intestinul subtire, strabat epiteliul mucoasei criptelor glandulare de la nivelul duodenului si jejunului si raman acolo pana ajung la maturitate, trecand prin 5 stadii larvare separate prin 4 perioade de naparliri.
Adultii revin in lumenul intestinal, si dupa acuplare, masculii mor, iar femelele vivipare patrund in peretele intestinal, unde depun 500‑1600 larve in ziua 6-7 dupa infectare. Acest proces continua pe tot cursul vietii femelei. Desi se considera ca, in general, formele adulte rezista in intestin doar pentru cateva saptamani, exista do ca pot supravietui pe perioade mult mai indelungate, in special daca sistemul imunitar al gazdei este compromis. Larvele tinere migreaza in lamina propria, patrund in vasele limfatice si sanguine, ajungand in circulatia generala care le transporta in tot organismul.
Evolutia este continuata numai de cele care ajung in muschii striati. In interiorul fibrei musculare, devenita celula doica, larvele cresc si se rasucesc in spirala. Miocitul are nucleul marit in volum, mitocondriile reduse ca volum, miofilamentele disparute, reticulul endoplasmatic proliferat. In mijlocul acestei celule hranitoare, larva dezvolta o capsula formata din doua straturi: unul intern, alcatuit din fibra musculara si o membrana exterioara, rezultatul unei reactii inflamatorii cu fibroblasti, macrofage si eozinofile. Capsula are deci, un caracter granulomatos. Dupa 4‑5 saptamani, larvele ajung la dimensiunea de 1 mm, iar procesul de inchistare este terminat. Cei mai infectati muschi sunt muschii diafragmului, laringelui, limbii, apoi intercostalii, maseterii, bicepsii, deltoizii si gastrocnemienii. Dupa aproximativ 5‑6 luni, chisturile se calcifica. Calcificarea chistului nu inseamna insa moartea parazitului. Sunt observatii din care rezulta ca parazitul ramane viabil in chist si pana la peste 40 de ani.
Se consemneaza prezenta mai multor specii de Trichinella: Trichinella spiralis (la porc, porc mistret, cal, urs, vulpe); Trichinella nativa (la mamifere terestre: urs, cal si mamifere acvatice); Trichinella britovi (la porc mistret, cal, rozatoare); Trichinella pseudospiralis (la pasari si mamifere omnivore); Trichinella nelsoni (la Hyenidae si Felidae).
Speciile Trichinella spiralis, Trichinella nativa, Trichinella nelsoni au un grad de infectare ridicat, in timp ce, la Trichinella britovi si Trichinella pseudospiralis, acesta este moderat.
Totusi, majoritatea specialistilor parazitologi considera valabile numai speciile de Trichinella spiralis si Trichinella pseudospiralis, in timp ce celelalte ar fi doar subspecii diferite sau tulpini.
Referindu-ne numai la Trichinella spiralis, organismele gazda pentru acest parazit se inscriu in doua cicluri evolutive: silvatic si sinantropozoonotic, conferind parazitozei caracterul de zoonoza.
In arealul nostru geografic, in ciclul silvatic intra: mistretul, lupul, ursul, vulpea, rozatoarele de camp, iar in ciclul zoonotic: porcii, sobolanii, soarecii, cainii, pisicile.
Daca in ciclul silvatic, infestatia este intretinuta prin necrofagie si canibalism, in ciclul sinantrop, un rol important il joaca porcul, consumator de sobolani infestati vii sau morti, cadavre de caini si pisici infestate.
De remarcat ca cele doua cicluri interfereaza la un moment dat, omul fiind consumator de carne de porc, porc mistret, urs si cal in foarte multe zone geografice.
Rezervorul de infectie
In trichineloza, sursa de infectie pentru om este in mod obisnuit porcul si mult mai rar, in functie de obiceiurile alimentare ale populatiei, alte animale, cum ar fi mistretul, ursul, cabalinele. Trichineloza se intalneste in randul acelor animale domestice sau salbatice la care e cunoscut canibalismul. Porcii intra in categoria acestora din urma, asa incat se pot infesta ingerand chisturile parazitului odata cu cadavrele sobolanilor.
Deficientele in orientarea si aplicarea deratizarilor sunt un factor de baza al scaparii de sub control al trichinelozei, mai ales cand nu este insotita de masuri gospodaresti in perioada efectuarii lor. Strangerea si indepartarea cadavrelor de sobolani trebuie efectuate inainte de a fi consumate de porci.
Un alt factor determinant al cresterii trichinelozei este administrarea unor supe de organe infestate in hrana porcinelor.
Caile de transmitere
Raspandirea trichinelozei in natura se face prin ingerarea carnii unei gazde parazitate de catre o alta gazda, din aceeasi specie, sau din alta specie.
Boala ajunge la om prin intermediul carnii de porc (sau de alte animale), atunci cand aceasta este consumata inainte de a fi in mod suficient preparata termic.
Masa receptiva
Receptivitatea omului fata de trichineloza este generala, boala intalnindu-se la ambele sexe si aproximativ la toate varstele. Majoritatea cazurilor de trichineloza la om, aparute in cursul anilor, au avut caracter de focare si episoade familiale, sau de grup (cantine, nunti, pomana porcului). Imbolnavirile au fost generate de carne si produse din carne de porc in stare cruda, sortimente obtinute prin sarare si afumare si preparate culinare, necontrolate in prealabil trichineloscopic.
Proportia cea mai ridicata de imbolnaviri apare in lunile de iarna, atingand punctul maxim la sfarsitul lunii decembrie, odata cu taierea masiva a porcilor din gospodariile populatiei si cu cresterea simtitoare a consumului de preparate traditionale din carne de porc ce poate proveni din surse neverificate sau de la producatori neautorizati.
Extinderea si intensitatea infectiei umane cu Trichinella spiralis sunt determinate de:
-prezenta in teritoriul considerat, al animalelor cu rol epidemiologic in infectarea umana si de potentialul lor de infectare.
-preferintele culinare ale populatiei, manifestate in modalitatile de preparare ale produselor din carne.
-masurile profilactice aplicate pe teritoriul respectiv, extinderea si eficienta lor.
Boala este raspandita in lumea intreaga, cu exceptia Australiei, fiind mai frecventa in emisfera nordica si in zonele temperate si reci. In Europa, trichineloza este considerata endemica in partea de rasarit.
In Romania, trichineloza a fost semnalata aproape pe toata suprafata tarii, mai ales sub forma de focare cu caracter familial, generate de consumul de carne de porc din gospodariile individuale.
Trichinella produce la toate gazdele animale tulburari digestive care intereseaza toate componentele anatomice (mucoasa, submucoasa, straturile musculare si mobilitatea, plexul mezenteric, structurile participante la transferurile ionice si reactogenitatea imuna locala).
Numeroase cercetari experimentale au stabilit ca localizarea enterala a parazitului Trichinella spiralis este echivalenta cu stabilirea unei nise ecologice. S‑a constatat ca larvele de prima generatie penetreaza si invadeaza monostratul epitelial ducand in final la alterarea si moartea acestor celule. Celulele enterale de la speciile natural parazitate (si de la animalele de laborator folosite ca model) au fost susceptibile, demonstrand spectrul larg in vivo al parazitului de a-si stabili nisa. Larvele depun antigen specific glicoproteic in celulele invadate si devin cea mai importanta tinta a anticorpilor care participa la eliminarea larvelor.
In mucoasa enterala are loc un proces inflamator reglat de moleculele mediatoare ale inflamatiei (molecule de adeziune, citokine, derivati ai acidului arahidonic).
Studii experimentale la rozatoarele infectate cu Trichinella spiralis au aratat ca, in fazele timpurii ale infectiei helmintice, atunci cand parazitul este prezent in tractul gastro-intestinal se induce o reactie de hipersensibilitate de tip I, ducand la cresterea nivelurilor de mastocite, eozinofile si producerea de IgE. Hipersensibilitatea imediata cutanata la antigenul larvar e observata in primele 3 saptamani de la infectare, concomitent cu producerea de IgE specific parazitare. IgE este principala Ig implicata in hipersensibilitatea imediata in bolile parazitare, helmintii fiind cei mai potenti agenti cunoscuti in stimularea producerii de IgE. La sobolanii infectati, Trichinella spiralis produce un raspuns specific parazitar de tip IgE, care s-a dovedit a fi protectoare fata de parazit, inclusiv in experimentele de transfer.
Trichinella spiralis induce o legare specifica pe intestin a IgE, mai intensa ca pentru G1, precum si un transfer crescut in lumenul intestinal (IgE>IgG1). In majoritatea modelelor experimentale, raspunsul imun implicat in eliminarea nematodelor e reglat de citokine produse de Th2 (in special IL-4).
Raspunsul imun indus de IL-4 regleaza productia de anticorpi si trecerea la izotipul Ig G1 < IgE precum si la activarea celulelor mastocitare. Transformarea limfocitelor B in plasmocite secretoare de Ig E e determinata de IL-4 si necesita ligandul CD 40. Sursa majora de IL-4 se considera a fi limfocitele Th care, dupa activare, exprima de asemenea ligandul CD40.
Raspunsul imun al gazdei consta in limitarea infectiei in diferite etape ale ciclului sau de viata. Rezistenta la Trichinella spiralis se asociaza cu expulzarea accelerata a viermilor adulti, diminuarea fecunditatii la femele si scaderea incarcaturii musculare.
Studii recente au demonstrat participarea IgE asupra mecanismelor efectoare care duc la eliminarea gastro-intestinala a nematodului precum si la reglarea in vivo a mastocitozei.
Cercetarile experimentale efectuate pe soareci au demonstrat ca infectia se coreleaza cu o crestere marcata a mastocitelor in intestin si splina. Hiperplazia mastocitara la nivelul intestinului subtire a fost observata la 7 zile de la infectie si a fost maxima in ziua 14. Cresterea mastocitelor in splina a inceput la 4 zile dupa infectie, persistand pe tot cursul experimentului.
Asupra activitatii motorii intestinale, Trichinella spiralis exercita in primele zile o crestere a contractiilor (5 zile postinfectie), cand se produce diaree si varsaturi. Aceasta este imun-mediata dependenta de limfociteleT si se realizeaza prin cresterea mieloperoxidazei.
Faza parenterala a infectiei cu Trichinella spiralis e asociata cu raspunsuri alergice si inflamatorii cauzate de invazia musculara a larvelor.
Miozita parazitara generalizata
Ajunse in teritoriul fibrei musculare, larvele difuzate de Trichinella spiralis isi formeaza o loja in sarcoplasma si initiaza transformarea miocitelor in celule gazda (nurse cells) care incep sa se inconjoare de vase capilare elaborate prin polimerizarea in situ.
Complexele vasculare apar doar in jurul miocitelor parazitate si se prezinta ca mici ducte anastomozate cu mari variatii de calibru. Parazitul induce angiogeneza, direct prin secretarea de produse, care actioneaza prin stimularea celulei loja (nurse), inducand proliferarea de celule endoteliale.
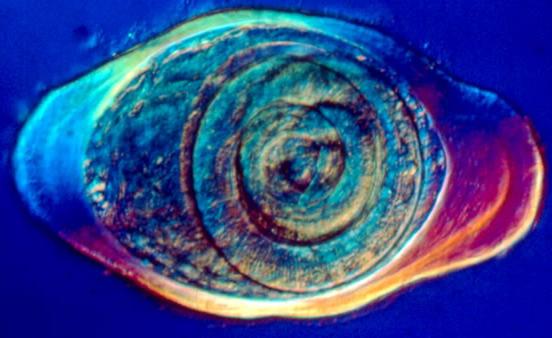
. 4. Complexul celula doica-larva
Invadarea celulelor muschiului scheletic de catre Trichinella spiralis duce la o modificare a ciclurilor metabolice, exprimata prin cresterea intensitatii dezasimilatiei (catabolismului), cresterea nivelului de proteinaze si fosfataze acide, inhibitia exprimarii lantului greu miozinic si mai tardiv, dezvoltarea de molecule de colagen distribuite catre zona de incapsulare.
Prin microscopie electronica, au fost urmarite stadiile de formare ale capsulei inconjuratoare in tesutul muscular la larvele de Trichinella spiralis. S‑a demonstrat ca miocitele produc ele insele, atat fibre de colagen, cat si glicoproteine si proteoglicani.
Produsele din partea interioara a capsulei sunt separate de cele din afara printr-o membrana bazala. Partea externa a capsulei contine fibre de colagen, sintetizate de celulele tesutului interstitial, de fibroblasti si de celulele endoteliului vascular.
Cardita trichinelozica
Mecanismul patogenic al miocarditei din trichineloza nu este bine cunoscut. In etapa actuala, se cunoaste gradul de participare a 4 procese fiziopatologice mai frecvente: inflamatia cu infiltratie eozinofilica, localizarea miocardica a larvelor (cu efecte patogenice directe sau mediate), substante mediatoare patogene (PAF platelet activating factor) sau prin mecanism imunopatogen (hipersensibilitate imediata, CIC agresive).
Larvele nou nascute de Trichinella spiralis se pot dezvolta in tesutul miocardic, dupa cum s-a demonstrat experimental la soarece. In modelul cel mai frecvent, obtinut dupa infestare, atat la prima infectie, cat si la reexpunere, se constata un bogat infiltrat cu eozinofile in leziunea miocardica, dar si dezvoltarea larvelor in cuiburi (care s-au identificat si in sistemul excito-conductor). Larvele nou‑nascute de Trichinella spiralis au putut fi recuperate frecvent din tesutul cardiac, dupa incubarea blocurilor de tesut in mediu suplimentar cu antibiotice, atmosfera 5% CO2 si 37C.
In alte conditii de mediu, recuperarea nu a fost posibila si s‑a ajuns la concluzia ca sunt necesare anumite conditii ambientale, pentru a se produce migrarea diferentiata in tesutul muscular cardiac, nervos si chiar pentru producerea leziunilor. Problema esentiala este daca leziunile cardiace se produc direct prin prezenta larvelor, sau de mecanisme mediate exercitate si la distanta.
In alte experimente, s-a recurs la inima izolata si perfuzata de sobolan, care anterior fusese contaminat cu Trichinella spiralis. Chiar din primele zile, s au cercetat indicii functionali cardiaci si s-a constatat o diminuare importanta a acestora (debitul cardiac, presiunea dezvoltata de VS, fluxul coronarian). Reducerea este si mai intensa daca, pe fondul infestarii, se administreaza o doza bolus de PAF (mediator arahidonic ce se elibereaza obisnuit la infestatie).
Intre alte actiuni pe care le exercita PAF, acesta e si activator eozinofilic si participant la numeroase leziuni cardio-respiratorii. Momentul de crestere maxima in sange a PAF si a eozinofiliei este dupa 21 de zile post infectie, ori, analiza prin AND helmintic proliferativ demonstreaza ca, dupa 21 de zile, modificarile morfologice si functionale din miocard nu mai pot fi puse pe seama prezentei parazitului, in acest stadiu este plauzibil a se admite ca, leziunile imunopatogen induse au rolul major in producerea leziunilor miocardice. In acest sens pledeaza si faptul ca, dupa 3 saptamani, unele celule inflamatorii (eozinofile si mastocite), apar in faza de degranulare, in curs de eliberare de mediatori.
Asocierea miocarditei cu neurotrichineloza este destul de frecventa. Participarea nervoasa a fost confirmata prin tomografie computerizata: semnele de encefalopatie, insotite frecvent de cele de deficit focal, au fost insotite de o moderata hipodensitate in cortex si substanta alba.
Sindromul cardio‑neurologic se dezvolta precoce si se coreleaza cu etapa de maxima eozinofilie. Semnele nervoase, care sunt atat difuze cat si focale, se asociaza uneori cu manifestari de infarct miocardic. Morfopatologic, post mortem s-a evidentiat micro‑tromboza arteriolara extinsa si leziuni ischemice focale in creier si miocard. Se banuieste rolul patogen al mediatorilor arahidonici si se evidentiaza raspunsul favorabil la corticosteroizi.
Eozinofilia
Numeroase investigatii au evaluat dinamic eozinofilia din trichineloza experimentala. S-au identificat doua varfuri: primul (cu o medie de 545+172,3 elemente) a fost corelat cu stadiul adult al parazitului, iar cel de-al doilea, mai pronuntat (cu o medie de 1265+334, 7 elemente) s-a corelat cu stadiul de migrare al larvelor. In etapa de incapsulare, se mai evidentiaza o crestere mai putin pronuntata, dar mai durabila. In genere, nu a existat o relatie neta de proportionalitate intre gradul invaziei musculare si eozinofilie.
O prima intrebare care s-a ridicat in legatura cu mecanismul eozinofiliei, a fost cea referitoare la modul de contact al maduvei hematogene, cu structurile antigenice ale Trichinellei. In acest sens, s-a cercetat raspunsul diferentiat, in functie de calea de administrare.
Soarecii infestati si inoculati i.v. cu larve omorate au dezvoltat in stadiul muscular o eozinofilie esential pulmonara cu inflamatie locala. La restimulare in vivo cu antigen de Trichinella spiralis, se produce o accentuare a raspunsului eozinofilic pulmonar, demonstrand ca expunerea la larve omorate (dupa infestare), genereaza efectiv memorie imunologica (deci activarea limfocitelor T cu memorie). In acest caz insa (la administrarea i.v. a antigenului), cinetica si caracteristicile raspunsului eozinofil sugereaza ca acesta se produce mai degraba prin redistributie locala, decat prin control sistematic (deci ca eozinofilogeneza indusa).
Argumentul major este acela ca, raspunsul dupa administrarea antigenica i.v. este diferita de cea dupa contaminarea orala cu Trichinella spiralis, cand modificarile importante din maduva osoasa sunt rezultatul stimularii formatiunilor receptor-imune din tractul digestiv, ceea ce duce la eozinofilopoieza cu cresterea numarului sanguin al eozinofilelor si al nivelului seric al IL-5. Asadar etapa enterala este obligatorie pentru eozinofilopoieza si posibil, pentru mecanismele patogenice la care eozinofilele sunt participante (prin incarcatura de mediatori ai inflamatiei si anafilaxiei).
Un alt context de investigatii au vizat relatia dintre mobilizarea eozinofilelor si rezistenta gazdei la infectia cu Trichinella spiralis. S-a procedat, in acest sens, la depletia macro organismului de eozinofile prin administrarea de anticorpi monoclonali anti IL 5 la soarecele infestat (de care depinde afluxul eozinofilic) si s a constatat ca aceasta nu modifica substantial incarcatura parazitara si nici rezistenta imunologica la reinfestare.
Totusi, nu s-au obtinut date convingatoare care sa demonstreze ca eozinofilele omoara formele de Trichinella spiralis infectante. Exista o scadere a parazitului in muschi, chiar in vivo, paralela cu mobilizarea eozinofilica, dar ramane valabila intrebarea daca aceasta este rezultatul unei actiuni direct paraziticide a eozinofilelor (exercitata la prima infectie sau la reinfectie) sau se incadreaza in mecanismele comune de aparare ale procesului inflamator in care si eozinofilele au partea lor de contributie.
Un alt studiu conchide ca eozinofilia contribuie la rezistenta la trichineloza, dar numai in etapa sistemica .
Diferentele importante existente, pe diverse modele, referitor la actiunea protectoare a eozinofilelor in trichineloza par sa se coreleze cu o inductie genetica. S-a demonstrat ca soarecele apartinand diferitelor suse, prezinta concomitent diferente, atat sub raportul raspunsului eozinofilic, cat si al rezistentei la Trichinella si al nivelului (variatiilor), eozinofilelor in splina si maduva osoasa.
Trichineloza, din punct de vedere clinic, se caracterizeaza printr-un polimorfism accentuat. Manifestarile bolii variaza in functie de numarul de larve ingerate, de tesuturile invadate, dar si de statusul imun al organismului afectat.
Incubatia bolii variaza de la 7 la 30 de zile si depinde de severitatea infectiei. In urma unei infectii severe, perioada de incubatie e mai scurta, insa s-au semnalat cazuri grave, urmate de deces, in asociere cu o incubatie lunga.
Etapa acuta a bolii se caracterizeaza prin doua faze: faza enterala in care parazitul altereaza functia intestinala si faza parenterala, asociata cu raspunsul inflamator si alergic la invazia musculara de catre larve.
Primele simptome gastro-intestinale rezulta in urma invaziei mucoasei de catre femelele adulte. Acestea dureaza, tipic, 2 pana la 7 zile, insa pot persista mai multe saptamani. Se declanseaza o enterita catarala cu hiperemie, edem al mucoasei si chiar mici ulceratii. In aceasta etapa, boala evolueaza cu diaree sau constipatie, greturi, varsaturi, dureri in etajul abdominal superior, stare generala alterata, febra. Diareea e mai frecventa decat voma, durand pana la 3 luni, determinand, in cazurile severe, deshidratare; deshidratarea asociata enteritei e o cauza de deces in aceasta etapa.
Acest tablou clinic e similar multor disfunctii enterale (de exemplu: toxiinfectii alimentare sau indigestie necomplicata), trichineloza fiind astfel greu de diagnosticat in aceasta etapa. In acest stadiu, pacientii nu apeleaza de obicei la medic, cerand asistenta medicala doar in momentul in care natura simptomelor se modifica, instalandu-se faza parenterala.
Faza parenterala corespunde diseminarii hematogene a larvelor, ceea ce declanseaza fenomene toxico-alergice. Aceasta faza se caracterizeaza prin afectare musculara, inclusiv miocardica; alte afectari posibile sunt afectarea nervoasa, pulmonara, renala si cutanata.
Sindromul trichinelozic se caracterizeaza prin edeme faciale, mialgii, febra, adinamie, mai putin intalnite sunt: anorexia, cefaleea, conjunctivita si urticaria. Febra e in general remitenta, apare in saptamana a doua de boala prezentand valorile cele mai ridicate in saptamana a IV‑a, ajungand pana la 40‑41C in cazurile severe. Pot apare semne oculare: edeme palpebrale, chemozis, conjunctivita, hemoragii conjunctivale, tulburari vizuale si dureri oculare. Edemele periorbitare sunt patognomonice, fiind probabil rezultatul raspunsului alergic.
In urma numeroaselor studii, cele mai intalnite simptome in formele usoare si moderate de trichineloza sunt reprezentate de: mialgii (30‑100%), polinevrite (10‑35%), edeme periorbitare, faciale (15‑90%), conjunctivita (55%), febra (30‑90%), cefalee (75%), rash cutanat (15‑65%), disfagie (35%), insomnie, scadere ponderala, parestezii, coriza, bronsita (5‑40%), hemoragii in aschie la nivelul unghiilor sau retinei, tulburari vizuale, paralizii ale muschilor oculari. Edemul poate cuprinde intreaga fata de unde si denumirea de boala capetelor umflate.
Mialgiile cuprind, cel mai frecvent, muschii extrinseci ai globului ocular, maseterii, muschii limbii si ai laringelui, diafragmul, muschii gatului si intercostalii. Mialgiile pot fi atat de severe, incat sa limiteze functional membrele, ducand la dificultati la mers, in timpul vorbirii (disfagie, disartrie), in timpul masticatiei sau al deglutitiei. Fatigabilitatea apare, de asemenea, ca o consecinta a afectarii musculare. Muschii devin rigizi, edematiati; edemul poate fi atat de accentuat incat sa simuleze hipertrofia. Edemul dureaza una pana la doua saptamani si se remite odata cu cresterea diurezei. Simptomele gastro-intestinale pot persista si in aceasta faza.
De multe ori, trichineloza evolueaza cu tulburari cardio-vasculare, neurologice, pulmonare, renale. Cea mai frecventa complicatie a aparatului cardio-vascular e reprezentata de miocardita, ducand uneori la stop cardiac; majoritatea deceselor care apar dupa afectarea cardiaca se produc intre saptamanile 4 si 8 de la infectie.
Diferitele tulburari de ritm cardiac apar secundar localizarii parazitului la nivelul tesutului excito-conductor. Modificarile EKG pot fi prezente incepand cu saptamana a II‑a si pot persista pana in saptamana 3 sau 4. Cele mai frecvente modificari sunt reprezentate de extrasistole, alungirea intervalului P-R, microvoltaj, bloc intraventricular, inversarea undelor T. Trichineloza poate lasa unele sechele miocardice, cel mai frecvent pot apare dupa cativa ani semnele insuficientei cardiace.
Tensiunea arteriala poate fi scazuta in prima parte a bolii si poate ramane scazuta in timpul convalescentei. Mai putin frecvent, se intalnesc in trichineloza si simptome vasculare precum epistaxis, hemoptizie, hemoragii digestive, tromboza arterelor femurala sau pulmonara si embolie. Tromboza poate aparea datorita unei stari de hipercoagulare asociata cu hipereozinofilia. Se mai pot intalni hemoragii petesiale, hemoragii in aschie subunghiale, precum si eruptii maculopapulare.
Destul de variate si numeroase sunt si tulburarile din partea aparatului respirator care pot insoti o trichineloza forma medie sau grava. Acestea pot fi determinate de o pneumonie sau pleurezie care se instaleaza in cursul evolutiei bolii. Bolnavii pot prezenta dispnee, tuse. Dispneea apare in principal datorita invaziei parazitare si inflamatiei consecutive a muschilor respiratori inclusiv diafragmul. Tusea se produce in urma trecerii larvelor prin patul capilar pulmonar, dupa aproximativ o saptamana de la infectie. Leziunile pulmonare de tip sindrom Lffler, cu caracter de congestie sau de vasculite alergice, se pot complica cu o suprainfectie.
Manifestarile neurologice, mai frecvente in infectiile severe, se intalnesc in 10‑24% din cazuri. Acestea apar, in special, la sfarsitul celei de‑a doua saptamani dupa infectie si sunt reprezentate de meningoencefalita (96%), paralizii sau pareze focale (73%), delir (71%), sau psihoze. Se mai intalnesc cefalee, vertij, tinitus, afazie, convulsii, modificarea ROT. Cefaleea e un simptom extrem de comun in trichineloza, durerea fiind exacerbata de miscarile capului. Meningita, encefalita sau plegiile, sunt determinate de distrugerea difuza a tesutului cerebral datorita ocluziei arteriolelor sau inflamatiei granulomatoase, necesitand tratament imediat cu steroizi. Mortalitatea, datorita, afectarii neurologice, e in scadere datorita cresterii eficacitatii tratamentului.
Datorita polimorfismului manifestarilor clinice, diagnosticul diferential se face cu: boala serului, edemul angioneurotic, septicemia, periarterita nodoasa, reactiile alergice, tromboza coronariana, febra tifoida, infectia cu Toxocara, bolile autoimune, sindromul eozinofilic, sindromul de oboseala cronica, poliomielita, meningita, encefalita, hemoragia cerebrala, pneumonia, bronhopneumonia, pleurezia, glomerulonefrita.
Simptomatologia asociata fazei acute diminua, progresiv, la instalarea convalescentei (cel mai frecvent in saptamanile 56 dupa ingestia carnii infestate).
Faza de inchistare a larvelor in musculatura incepe din saptamana a 3-a de boala si dureaza pana in saptamana a 7-a. Reprezinta tot o perioada critica, deoarece larvele nu sunt complet izolate si toxinele lor pot disemina in organism. Mialgiile persista si desi edemele incep sa regreseze, bolnavul devine casectic, casexia putand conduce la deces. Dupa acest interval, riscul evolutiei letale scade, manifestarile clinice se amelioreaza treptat.
Existenta trichinelozei cronice, sau sechelare (persistenta mialgiilor, fatigabilitatii, simptomelor oculare, cefaleei) e o problema controversata, care necesita investigatii suplimentare.
Unul dintre studiile conduse in acest sens de catre Harms G, constata ca, la 10 ani de la izbucnirea epidemica a infectiei cu Trichinella spiralis, se pot evidentia urmatoarele modificari clinico-biologice (la 128 persoane):
- simptome musculare (90%)
- simptome oculare (inclusiv conjunctivita) (5559%)
- simptome neurologice (52%)
- simptome psihice (52%)
Manifestari particulare:
- scaderea demonstrata biologic a fortei musculare (56%)
- alterari de coordonare (32%)
- prezenta Ac specifici Ig G la Trichinella spiralis (38%)
Complicatiile care apar in timpul bolii acute includ avort spontan, sau transmiterea verticala a infectiei la pacientele insarcinate.
In timpul convalescentei, pacientii acuza tulburari de auz, scadere ponderala, modificari ale ciclului menstrual, descuamarea pielii, caderea parului si a unghiilor, rigiditate musculara.
Desi in zilele noastre, decesul se produce rar in trichineloza datorita eficacitatii tratamentului, poate apare in urma stopului cardiac secundar miocarditei, encefalitei, pneumoniei, hipokaliemiei, insuficientei corticosuprarenalei.
Trichineloza nu se manifesta de fiecare data cu o simptomatologie clinica evidenta. Exista in trichineloza, ca si in alte boli parazitare, forme asimptomatice, subclinice, care trec total neobservate. Numarul unor asemenea purtatori sanatosi este uneori destul de mare. Apreciate dupa eozinofilia moderat crescuta si dupa faptul ca era vorba de persoane care consumasera din aceeasi carne infestata, din care au mancat bolnavii deja cunoscuti, s-au descoperit in unele focare cercetate din punct de vedere epidemiologic ca numarul acestora trecea uneori de 50%.
Un loc destul de important il ocupa, intre formele clinice ale bolii, formele usoare care adeseori nici nu solicita asistenta medicala. Multe din cazurile de trichineloza evolueaza ca forme medii de boala, atunci cand bolnavii au o simptomatologie evidenta: febra, edeme faciale, palpebrale, mialgii si care necesita asistenta medicala de specialitate.
In trichineloza, mai mult decat in alte boli parazitare, se intalnesc si forme grave, intrunind 15‑20% din cazurile de boala. Alti autori deosebesc in trichineloza forme clinice tipice si atipice. Formele clinice tipice sunt constituite din cazurile la care se intalnesc simptomele obisnuite ale bolii, iar formele atipice sunt reprezentate de acele cazuri, in care se prezinta numai o parte din simptomele bolii, in rest imbracand aspecte cu totul aparte.
Diagnosticul in trichineloza, in cazurile izolate, in afara unui focar epidemiologic si atunci cand nu este luata in discutie o anumita sursa de infectie, este un diagnostic dificil. O maladie cu o evolutie atat de diferita si cu un polimorfism clinic atat de accentuat, sugereaza o multitudine de alte boli.
O atentie deosebita trebuie acordata anamnezei, in special obiceiurilor alimentare din saptamanile anterioare instalarii simptomatologiei. Expunerea la carne infestata, prezenta gastroenteritei, mialgiile, edemele faciale, hemoragiile subunghiale si conjunctivale, impreuna cu cresterea eozinofilelor, ar trebui sa sugereze trichineloza. Confirmarea bolii se realizeaza prin intermediul explorarilor paraclinice.
Evidentierea parazitilor adulti in scaun, in faza de invazie, este dificila. Momentul depistarii, in scaun, incepe la 3 zile de la ingerarea carnii infestate si se intinde pe parcursul a cel putin 3 saptamani de la infestare. Proba nu este foarte certa, intrucat in momentul aparitiei semnelor clinice, numarul parazitilor adulti din intestin incepe sa scada. Se examineaza proba din scaunul diareic, eventual dupa administrarea unui purgativ salin. Rezultatul negativ nu infirma diagnosticul.
Metoda Staubli vizeaza decelarea larvelor in sange (mai rar in LCR, exudate pleurale sau peritoneale), incepand din a 2-a si a 3-a saptamana de boala. Se amesteca 10 ml sange cu 100 ml acid acetic 30%. Amestecul se centrifugheaza, iar larvele se cauta in sediment. Se poate face si un frotiu colorat MGG. Metoda nu da rezultate reproductibile si nu a intrat in practica curenta. Rezultatul negativ nu infirma diagnosticul.
Biopsia musculara este metoda cea mai sigura pentru confirmarea diagnosticului, dar ca urmare a electivitatii pe care o prezinta parazitul pentru anumite grupe musculare, proba poate ramane negativa, in special in infectiile mici sau medii. Biopsia se practica la 3‑4 saptamani de la infestare, in muschiul solear (gastrocnemian), in vecinatatea tendonului lui Ahile, sau din muschiul deltoid, biceps. Fragmentul recoltat trebuie sa fie de dimensiuni suficient de mari.
Parazitul se poate prezenta sub forma de larve libere, larve spiralate, iar din luna a 2-a de boala, larve incapsulate. Chisturile calcificate apar mult mai tarziu si semnalarea lor are valoare de diagnostic retrospectiv.
In practica medicala curenta se utilizeaza urmatoarele 3 metode: trichineloscopia, examenul histopatologic si digestia artificiala.
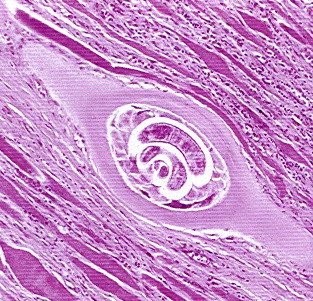
. 5. Larva de Trichinella spiralis in sectiune musculara
Trichineloscopia (examenul direct): fragmentul de muschi se comprima intre doua lame, care se fixeaza la capete cu doua cleme. Se examineaza la microscop, rezultatele fiind dependente de momentul efectuarii biopsiei, raportat la momentul infectarii. In prima saptamana, identificam larva libera intre fibrele musculare, in saptamana a 3‑a, larva spiralata in fibra musculara, iar din saptamana a 5‑a, larve incapsulate caracteristice. Chisturile calcificate apar la cel putin 5-6 luni de la infectie.
Examenul histopatologic: fragmentul de muschi ce urmeaza a fi examinat se sectioneaza la microtom dupa o prealabila fixare si includere in parafina.
Digestia artificiala: metoda consta in izolarea larvelor de Trichinella spiralis, din fragmentul muscular recoltat cu ajutorul sucului gastric preparat artificial (folosind in acest scop pepsina si HCl). Nu pune in evidenta larvele sub 17‑18 zile post‑infectie si nici pe cele moarte, cu modificari alterative profunde, deoarece se distrug in cursul procesului de digestie. Efectuata corect, metoda ofera rezultate superioare examenului trichineloscopic. In vederea unei bune eficiente a digestiei artificiale, se va tine cont ca larvele se acumuleaza preferential in limba, muschii gatului, supraspinos, trapez, diafragm. Se recomanda probe de 5‑10 grame.
Metoda biopsiei musculare permite un diagnostic pozitiv in aproximativ 50% din cazuri, rezultatul ei fiind conditionat de intensitatea infectiei, de momentul efectuarii biopsiei, in raport cu data infectarii si de dimensiunea fragmentului de muschi prelevat. O biopsie pozitiva certifica existenta infectiei actuale sau in antecedente, dar una negativa nu infirma diagnosticul. Metoda are urmatoarele limite:
- evidentiaza larvele numai dupa 17‑20 de zile de la infestatie.
- in caz de infestatie redusa, rezultatul poate fi negativ sunt necesare in acest caz 28 sectiuni in loc de 14.
- diagnosticul pozitiv de certitudine se obtine in cel putin 50% din cazuri.
Examenul la microscopie electronica pune in evidenta ultrastructura tesutului lezat, dar permite si intelegerea circuitului parazitului in organism si mai cu seama formarea nisei ecologice. Dupa penetrarea larvei in sarcoplasma celulei musculare, se produce transformarea bazofila a acesteia si se formeaza complexul locas (nisa) larva-celula.Sunt identificate 3 tipuri de larve:
- tipul I (L1) cu vechime de o ora
- tipul II (L2) cu vechime de 9 ore
- tipul III (L3) cu vechime de 6 zile
In vecinatatea celulei parazitate, se produce o reactie inflamatorie cu aflux de proteine de faza acuta si citokine (limfokine, IL-l, IL-4, IL-5, TNF).
Deseori, cercetarea ultrastructurala se completeaza cu studii histoenzimatice. Cel mai des a fost investigata cresterea activitatii proteinelor si modificarile in diverse etape ale bolii. Se obtine o curba ascendenta intre saptamanile 1 5, dupa care urmeaza o usoara diminuare. Proportionalitatea intre cresterea proteinazelor si intensitatea leziunilor histopatologice este evidenta.
Superoxiddisimutaza in izolatele de Trichinella spiralis, enzima ce actioneaza asupra radicalilor liberi, a fost evidentiata si in vitro (prin analiza El Fo), dar si in vivo prin histochimia muschiului infestat. Este pronuntat crescuta in capsula si in stratul de aderare directa .
Examene de laborator nespecifice
Hemoleucograma: modificarea caracteristica trichinelozei este hiperleucocitoza cu valori cuprinse intre 15‑30.000/mmc cu neutrofilie si moderata deviere la stanga, o proportie importanta a leucocitelor fiind reprezentata de eozinofile, cu procente cuprinse intre 15‑90%.
Eozinofilele concura alaturi de alti factori la apararea nespecifica a organismului, avand o capacitate mai redusa de fagocitare decat neutrofilele. Rolul primordial este de a neutraliza mediatorii produsi de mastocite si bazofile. Se constata o crestere brusca a eozinofilelor in sangele periferic incepand cu ziua a sasea de la infectia cu Trichinella spiralis. Eozinofilia apare in faza de migrare a parazitului si atinge maximum de 60‑90% in faza de invazie musculara. Media se incadreaza intre 30‑40%. Nivele ridicate pot fi remarcate uneori pe o perioada mai indelungata, chiar de ordinul anilor.
In cursul bolii, se dezvolta eozinofile hipodense, care sunt mult mai toxice pentru larvele de Trichinella decat eozinofilele normodense. Toxicitatea eozinofilelor pentru larvele tinere este demonstrata prin prepararea unui extract de epiteliu intestinal care contine mastocite si eozinofile si punerea lui in contact cu larvele tinere de Trichinella spiralis.
La sobolan si la om, aceste celule adera de larvele L1 si impiedica patrunderea lor in muschi. Unii autori mentioneaza ca eozinofilele adera si omoara numai larvele tinere, printr-un mecanism dependent de anticorpi si independent de complement.
Hipereozinofilia se poate mentine o perioada variabila de timp, de la cateva saptamani pana la 1‑2 ani (media de 6 luni). Descresterea numarului de eozinofile se face la inceput brusc, apoi progresiv. In evolutia acuta, o scadere brusca a eozinofilelor indica o forma clinica severa.
Intr-un numar relativ redus de cazuri, numarul total de leucocite poate fi in limite normale, modificari prezentand doar formula leucocitara cu cresterea procentului de eozinofile.
Numarul de hematii se mentine in limite normale. Daca, insa, evolutia bolii este prelungita, de cele mai multe ori, apare o anemie hipocroma. VSH-ul poate fi in limite normale sau usor crescut.
Examene biochimice
Agresiunile infectioase, virale, microbiene sau parazitare, pot modifica procesele oxidativ‑energogene ale celulelor afectate in cazul in care scad aportul oxigenului sau blocheaza etapele de utilizare a acestuia in ciclul oxidativ. In faza musculara a trichinelozei, ambele mecanisme inductoare se confirma.
In cazul in care cele doua circumstante cauzatoare sunt valide, asistam la secventializarea a 3 etape:
I. Prima etapa este cea in care aportul si utilizarea celulara a oxigenului decurg in limite normale. In aceasta situatie, nu e afectat angrenajul glicoliza oxidatie celulara (in special ciclul acizilor carboxilici Krebs) - fosforilare oxidativa (producerea legaturilor fosfatice macroergice materializate prin ATP, ADP si CP).
II. Etapa a doua este cea in care aportul sau utilizarea celulara a oxigenului diminueaza, ca urmare a hipoxiei moderate sau blocului oxidativ, asa cum se intampla in trichineloza.
In 1861, Pasteur a constatat ca levurile descompun glucoza la acid lactic, mai lent in conditii aerobe decat in conditii anaerobe. Transpus la celulele animale, efectul Pasteur poate fi enuntat astfel: in cazul in care aportul de O2 este diminuat, este activata glicoliza anaeroba care, desi are un randament energetic mult mai redus decat glicoliza aeroba, poate suplini, in anumite limite, productia aeroba prin ritmul sau accelerat.
Adaptarea tesuturilor la efectul Pasteur este diferentiata. Celulele SNC pot creste ritmul de 10 ori, celulele hepatice de 7 ori, dar muschiul scheletic are o capacitate compensatorie mult mai redusa (de 24 ori), mai ales daca afectarea este extinsa, asa cum se intampla in miozita trichinelozica. Lactatul, piruvatul si fosfatul organic sunt, fie in limite normale, fie moderat in afara acestora.
III. Etapa a treia se instaleaza atunci cand mecanismul compensator, prin accelerarea glicolizei, se epuizeaza, ca urmare a scaderii drastice a O2 sau a blocului oxidativ (prin actiunea toxinelor parazitare). In acest caz, apare efectul Pasteur inhibat, care se defineste prin:
-ritmul si intensitatea glicolizei anaerobe depaseste cu mult ritmul si intensitatea oxidatiei
-bilantul energetic celular si circulant devine negativ, deoarece oxidatia nu mai reuseste sa sustina fosforilarea oxidativa, ca atare scade concentratia celulara si circulanta a compusilor macroergici (ATP, ADP, CP)
-predomina catabolismul (dezasimilatia), asupra anabolismului, prin scaderea biosintezei proteice energo-dependente
-este alterat transferul ionic transmembranar energo dependent cu depletia K intracelular si hiperkaliurie
Astfel, cea mai importanta modificare functional biochimica ce sta la baza miozitei parazitare generalizate in trichineloza este alterarea concomitenta a oxidatiei celulare si a fosforilarii oxidative, cu cresterea lactatului seric, cu tendinta la acidoza lactica, cresterea piruvatului seric, modificarea raportului L: P si scaderea fosforului organic.
Subeficienta procesului oxidativ‑energogen determina un grad de hipercatabolism proteic insotit de o diminuare a biosintezei proteice. Hipercatabolismul se exprima prin hipoproteinemie cu cresterea creatininei si prin hipokaliemie cu hiperkaliurie.
In urma leziunilor musculare, cresc enzimele musculare (CPK, LDH, aminotransferazele), la 35‑100% din pacientii infectati.
Complexele imune circulante se asociaza patogenic cu formele severe de boala si posibil cu patogenia miocarditei trichinelozice.
Raspunsul imun in trichineloza
In majoritatea etiologiilor parazitare, raspunsul imunologic al gazdei este subeficient, ceea ce explica persistenta mai indelungata a infectiei. Pentru explicarea acestui fenomen, s-au invocat mai multi factori:
-stimularea eliberarii de hormoni corticosteroizi imunosupresori
-incapsularea agentului parazitar, ceea ce face dificil accesul anticorpilor
-producerea de catre parazit a unor factori limfocitotoxici (dovedit in vitro pentru Trichinella spiralis)
-eliberarea de catre paraziti a unor substante ce actioneaza ca activatori policlonali ai limfocitelor cu pierderea capacitatii limfocitelor de a elabora raspuns imun specific.
Mai probabil este insa, ca factorul principal este reprezentat de variatiile rapide in structura antigenica a parazitului. Metazoarele prezinta in jur de 60 de structuri antigenice interne, cuticulare si excretate. Cele cuticulare, fiind in contact permanent cu tesuturile gazdei, determina raspunsuri imune pe tot parcursul vietii parazitului, dar cu eficienta redusa, deoarece efectorii imuni se adreseaza unor stadii antigenice anterioare si depasite. Pe de alta parte, din numeroasele antigene parazitare, numai un procent redus dintre ele sunt imunogene.
Imunitatea umorala are o actiune protectoare redusa: numai 5‑6% din anticorpii formati au efect antiparazitar. Imunitatea celulara actioneaza, mai ales, asupra stadiilor primare de dezvoltare.
Mecanismul imun parazitar se dezvolta bifazic:
-in prima etapa, actioneaza imunoglobulinele specifice care produc leziuni degenerative asupra citoplasmei si alterari enzimatice (reactia asigura cooperarea cu complementul, dar nu asigura eliminarea parazitului).
-in a doua etapa, intervin limfocitele T sensibilizate care pot contribui la expulzarea parazitului, numai daca s-a produs faza anticorpica.
Drept urmare a acestor mecanisme, cu caracter variabil, in parazitoze se intalnesc urmatoarele 4 alternative:
-absenta oricarei imunitati castigate (ex. Entamoeba histolitica)
-imunitate nesterilizanta (in toxoplasmoza)
-imunitate de etapa, care priveste numai formele de invazie, nu si cele adulte
-imunitate sterilizanta in Trichinella spiralis. Distrugerea parazitului este produsa prin actiunea cooperanta a anticorpilor specifici Ig M, eozinofilelor si limfocitelor T activate.
La bolnavii de trichineloza se evidentiaza insa si reactii imun agresive, apartinand urmatoarelor categorii:
- reactii de hipersensibilitate de tip imediat, care apar in faza de migrare sangvina a larvelor (eliberarea de mediatori cu actiune farmacodinamica de tip histaminic). Raspunsul imun de tip alergic, cu decelarea unor titruri serice crescute de IgE, este individual si nu pare a fi concordant cu severitatea simptomelor clinice.
- reactii cu leziuni prin complexe imune, care, activand complementul, declanseaza o serie de evenimente celulare si umorale, cu efecte histotoxice la locul depunerii. Complexele imune sunt implicate in leziuni ale peretelui vascular, in producerea edemelor si necrozei celulare.
- reactii de hipersensibilitate intarziata, cu mediere celulara, sub influenta limfokinelor.
Antigenitatea indusa de Trichinella spiralis in organismul parazitat, ca larva si parazit adult, se exprima sub 2 forme:
- antigene somatice, continute in extractul corpului parazitului
- antigene metabolice, prezente in secretii si excretii
Atat antigenele somatice, cat si cele metabolice, sunt mai puternice la larve decat la adulti, iar la ambele forme evolutive, antigenele metabolice sunt mai active decat cele somatice.
Larvele de Trichinella spiralis au 19 fractiuni antigenice, cu doua caracteristici implicate in diagnosticul serologic:
- variabilitate antigenica in timp: larvele de varsta diferita au structuri antigenice variate, necesitand o specificitate antigenica cat mai mare, pentru un diagnostic serologic cat mai fiabil
- interfereaza cu antigene de alti paraziti: Fasciola, Ascaris, Echinococus (se inregistreaza astfel reactii incrucisate si fals pozitive).
Larvele migratoare si formele adulte ale parazitului exprima antigene responsabile de protectia in fata unei noi infestatii.
O expresie importanta a rezistentei organismului gazda este reprezentat de expulzia rapida a parazitilor aflati in cursul dezvoltarii, sau a celor adulti, de la nivelul intestinului organismului parazitat, reprezentand asa numitul fenomen de autovindecare (self-cure phenomenon); acesta se produce in conditiile in care o noua infestatie initiaza un raspuns din partea organismului gazda, producand eliminarea infestatiei anterioare, fenomen aparent opus celui reprezentat de raspunsul imun concomitent.
Larvele migratoare si adultii exprima antigene ce pot sa devina responsabile de protectia fata de noi infestatii, tocmai prin acest procedeu de self cure. Expulzia Trichinellei spiralis in gazda umana se desfasoara in doua etape:
- alterari metabolice ale parazitului, induse de anticorpi
- expulzia parazitului prin intermediul limfocitelor T activate poliantigenic.
Raspunsul imun umoral la Trichinella spiralis implica aparitia de anticorpi Ig M, urmat de raspuns Ig G, dar si anticorpi Ig A (mucoasa intestinala) si Ig E. La nivel intestinal, se produce cresterea nivelului de Ig A si Ig M. Aceasta reactie este directionata selectiv fata de parazitul aflat in faza de dezvoltare si maturare (feeding parasite), este independenta de complement si precede expulzia rapida, mediata prin intermediul limfocitelor T, a parazitilor alterati de catre actiunea respectivilor anticorpi.
Prepararea antigenelor
Dupa cum s-a aratat, ca orice metazoar, Trichinella spiralis contine un mozaic de antigene. Acestea nu au importanta diferentiata numai in stabilirea raspunsului imun al gazdei, dar si in delimitarea semnificatiei diagnostice a probelor imunologice, care necesita, un grad ridicat de sensibilitate si specificitate.
Antigenul larvar purificat de Trichinella spiralis, cu mare afinitate si specificitate, se obtine prin trecerea antigenului crud somatic de muschi larvar, prin coloana de gel cu Ig G - antitrichuris suis. Substanta obtinuta contine 7 antigene cu MM intre 28‑35 KDa. Acesta s-a dovedit mai specific decat majoritatea celorlalte antigene somatice, care dau reactii fals pozitive si cross‑reactii.
O alta procedura de studiere a antigenitatii muschiului de larve de Trichinella spiralis, in vederea utilizarii in imunodiagnostic, a constat in obtinerea de sectiuni ultrafine de larve fixate, care au fost tratate cu ser, la pacientii cu o varietate de infestatii parazitare, incluzand si trichineloza; amestecul a fost tratat cu protein- A- aur coloidal. Tehnica permite demonstrarea ca, suprafata cuticulara si granulele stichocite, poseda o specificitate proprie in producerea anticorpilor anti Trichinella spiralis.
S-au utilizat si anticorpii monoclonali, pentru izolarea antigenelor specifice de Trichinella spiralis, pentru o buna afinitate cu ELISA si WESTERN BLOT, aratandu-se ca sunt glicoproteine.
Deosebit de bine sunt evaluate antigenul purtator de fosforolcolina (PC) si antigenul ES (excreto-secretor). Antigenul ES se obtine din larve cultivate pe muschi si este utilizat mai ales intr-o varianta ELISA, ca test serologic rapid, pentru imunodiagnosticul trichinelozei porcului. Are un indice diagnostic de 98%, fals‑pozitivitate de 3% si necesita a tine permanent animale de laborator parazitate, pentru a produce compusul. Molecular, a fost exprimat si genetic, pe baza secventelor ADNc si s-a constatat a fi o proteina de 53 KDa.
Alti autori au obtinut un antigen ES de 76KDa, similar ca reactogenitate cu cel obtinut cu anticorpi monoclonali, de asemenea cu inalta afinitate si specificitate. Are structura polipeptidica, da rezultate bune la ELISA si e recunoscut la Western Blot.
Antigenele diagnostice, care contin fosforilcolina (PC), se obtin prin procedeu cromatografic, utilizand anticorpi monoclonali. Componentul cel mai eficient antigenic are o MM de 45KDa si pare a fi molecula esentiala a produsului ES (excreto-secretor), al muschiului larvar. Utilizat in ELISA, are specificitate echivalenta cu aceasta. Inoculat la soarece, produce IgManticorp specific PC. Infectia cu Trichinella spiralis poate supresa raspunsul la alte antigene purtatoare de PC, datorita, unui factor solubil, prezent in serul animalului infestat, care este o IgG1.
Intradermoreactia
Din antigenul obtinut din larvele parazitului, se injecteaza intradermic, pe suprafata anterioara a antebratului, 0,1 ml antigen diluat 1/1000. Reactia imediata se citeste dupa 1020 minute si consta intr‑o papula alb‑roz, inconjurata de o zona eritematoasa, usor edematiata. Reactia tardiva apare dupa 10‑24 ore, este asemanatoare, avand un diametru de 2‑3 cm. Dintre cele doua forme de reactie, cea imediata are o valoare superioara de diagnostic.
Testul cutanat este, in general, destul de sensibil si poate fi folosit in diagnostic, din a doua saptamana de boala. Sensibilitatea fata de antigen se mentine timp indelungat, rezultatul pozitiv putand fi determinat si de o infestare mult mai veche (teste epidemiologice).
Reactia de precipitare circumlarvara (RPL ROTH)
Metoda foloseste, ca antigen, larve liofilizate, sau larve vii, obtinute prin digestie peptica, de la animale (cobai), infestate in laborator. Aproximativ 100 de larve, dupa ce au fost spalate cu ser fiziologic steril si cu penicilina si streptomicina, sunt asezate intr-un godeu de 0,5‑1 ml, alaturi de 0,5‑1 ml ser, provenit de la bolnavul suspect. Lama se aseaza la 37 grade in camera umeda. Citirea se face dupa primele doua ore si apoi zilnic, timp de cinci zile.
Rezultatele pozitive sunt date de precipitatele microscopice, care apar in jurul orificiilor bucale si anale ale larvelor. Intensitatea reactiei este in functie de cantitatea precipitatelor formate si de mortalitatea larvelor, se noteaza cu + ‑ + + + +. Rezultatele pozitive apar dupa 10‑20 zile de la infestare, ating maximum intre zilele 45‑65 si se mentin pana la aproximativ un an de la infestare.
Reactiile de aglutinare
Aglutinarea cu colesterol (Sussenguth Kline)
Metoda foloseste, ca antigen, un extras alcalin larvar, absorbit pe particule de colesterol. Reactia se efectueaza, adaugand la 0,5 ml ser inactivat, introdus in prealabil intr-o celula parafinata, o picatura din antigenul de mai sus. Dupa ce lama a fost rotata timp de 4 minute, cu o frecventa de 100 ture/minut, se face citirea la microscop a preparatului. Rezultatele pozitive sunt date de aglutinarea particulelor de colesterol. Actualmente se folosesc antigene liofilizate.
Aglutinarea cu bentonita (Bozicevich)
Metoda foloseste absorbtia extractului de Trichinella spiralis, pe particule de bentonita. Se utilizeaza antigen liofilizat. Particulele de bentonita, acoperite cu antigen, sunt amestecate, pe o lama, cu variate dilutii din serul inactivat la cald, al suspectului de trichineloza. Flocularea particulelor este citita la microscop, rezultatul fiind notat de la 0 la + + + +, confruntarea cu martorul fiind obligatorie.
Comparand sensibilitatea si specificitatea acestui test cu hemaglutinarea si imunofluorescenta indirecta, s-a constatat ca BFT a fost mai sensibil si mai specific, deoarece a fost singurul care nu a dat reactii fals pozitive. BFT ramane pozitiv 3 5 ani de la infestatie. Dezavantajul major este incapacitatea de a detecta anticorpii timpuriu in timpul infectiei, in special in cazurile de proportii mici si moderate.
Reactia de hemaglutinare
Testul foloseste, ca antigen, fractiunea proteica acidosolubila, iar pentru vehicularea acesteia se utilizeaza hematii tanate. Pe hematiile tratate cu acid tanic, se absoarbe antigenul solubil. Hematiile, invelite cu antigen, se adauga la serii de dilutii din serul recoltat de la bolnav si se fixeaza tipul de anticorp. Metoda este specifica si sensibila (numar mare de rezultate pozitive).
S-a utilizat si un test de hemaglutinare indirecta (HAI) care, intocmai ca majoritatea probelor rutiniere, a fost evaluat prin are cu testul clasic de precipitare (TP) si testul de floculare cu bentonita. Indicele de pozitivitate a fost de ~ 80% (abil cu celelalte doua), dar autorii considera ca prin asocierea lor (nu prin opunere), se acopera o arie diagnosticata apropiata de 100%.
Reactia de fixare a complementului
Este o metoda serologica de titrare a anticorpilor, dintre cele mai sensibile Se utilizeaza antigene polizaharidice acidosolubile, care se incubeaza, impreuna cu dilutii din serul bolnavului si cu o cantitate determinata de complement. Drept indicator al fixarii sau nefixarii complementului, se folosesc hematii de berbec, sensibilizate cu ambocaptor (ser hemolitic).
In cazul in care, serul controlat nu contine anticorpi, complementul nefixat va produce hemoliza hematiilor sensibilizate si vom avea un rezultat negativ. Daca, din contra, serul prins in control, contine anticorpi, complementul se va fixa pe sistemul antigen‑anticorp si drept urmare, nu va mai apare hemoliza, ceea ce este egal cu un rezultat pozitiv. Anticorpii fixatori de complement, apar la 2‑3 saptamani dupa infectare si persista 2‑3 luni.
Reactia de imunofluorescenta
Principiul metodei se bazeaza pe faptul ca, anticorpii combinati cu o substanta fluorescenta (izotiocianatul de fluoresceina), isi pastreaza reactivitatea imunologica. Izotiocianatul de fluoresceina are calitatea de a produce, in lumina ultravioleta, o fluorescenta stralucitoare. Ca antigen, se folosesc larvele parazitului, fixate in formalina, tratate cu serul bolnavului si puse in contact cu ser antigamaglobulina umana, marcata cu izotiocianat de fluoresceina. Reactia poate fi efectuata prin doua metode:
- metoda directa, consta in punerea in contact a antigenului cu serul fluorescent specific;
- metoda indirecta, consta in punerea in contact, in prima etapa, a antigenului cu anticorpul specific nefluorescent. In urma cuplarii antigenului cu anticorpul, nu se produce o reactie fluorescenta. In faza a doua, cuplul antigen-anticorp este pus in contact cu un anticorp fluorescent.
Reactia este destul de sensibila si este, mai ales, utila in diagnosticul cazurilor subclinice si asimptomatice. Rezultatele pozitive ajung pana la o proportie de 95‑98%, dar pot apare si reactii fals pozitive.
ELISA (Enzimolinked immunosorbent assay)
Reprezinta, in etapa actuala, cel mai sensibil test de diagnostic serologic in trichineloza. Consta in detectarea anticorpilor, sau a antigenelor, prin intermediul enzimelor, folosind reactia clasica antigen‑anticorp. In principiu, in efectuarea testului, se deosebesc urmatoarele etape:
- fixarea antigenului sau a anticorpului, pe un substrat solid;
- cuplarea elementului fixat pe suport, cu elementul de identificat (anticorpul sau antigenul), din proba de examinat;
- evidentierea complexului antigen anticorp, eventual format, cu ajutorul unui al doilea antigen sau anticorp, cuplat cu o enzima;
- adaugarea, in final, a substratului specific enzimei folosite drept marker si vizualizarea sau determinarea cantitativa a prezentei anticorpului sau antigenului cu o enzima, indicator al reactiei, prin actiunea enzimei asupra substratului corespunzator.
Testul are mai multe variante, dar cele mai utilizate sunt:
- metoda indirecta, prin decelarea anticorpilor;
- metoda directa;
- metoda dublu anticorp sau sandwich pentru evidentierea antigenelor.
Suportul solid, pe care se realizeaza absorbtia antigenului sau anticorpului, este confectionat din mase plastice, sub forma de placi cu godeuri, tuburi sau perle (din polistiren, nylon) sau discuri de hartie, activate cu CNB sau CNB Sephadex, tiol Sepharose.
Antigenul poate fi reprezentat de extracte de larve sau produse de secretie si/sau excretie.
Anticorpii necesari pot fi de doua feluri: specifici fata de antigenul folosit in reactie, fiind prezenti in serul pacientilor de cercetat sau in serul unor animale infestate experimental cu antigenul corespunzator si anticorpi (antiimunoglobuline de specie), fata de imunoglobulinele speciei de la care provine anticorpul de identificat sau fata de imunoglobulinele pe care s-a preparat anticorpul specific fata de antigenul de identificat.
Markerii (labilizati) sunt enzime ca: fosfataza alcalina, peroxidaza, glucosidaza si beta‑galactosidaza. Acestea se cupleaza cu elementul ce urmeaza a fi marcat, prin intermediul unui agent de cuplare (ex.: glutaraldehida), realizandu‑se conjugatul antigen‑enzima sau anticorp‑enzima.
In metoda ELISA directa, se foloseste conjugatul anticorp‑enzima, obtinut prin marcarea anticorpilor specifici antigenului conjugat globulinic specific.
In metoda ELISA indirecta si dublu sandwich, se foloseste conjugatul antiimunoglobulinic de specie, obtinut prin marcarea antiglobulinelor de specie (om, porc, cal).
Substratul specific enzimei folosite, este reprezentat de paranitrofosfat pentru fosfataza alcalina, acid 5-aminosalicilic sau ortofenilendiamina, pentru peroxidaza.
Interpretarea se face prin determinarea activitatii enzimei, din conjugatul legat asupra substratului, citita colorimetric (la spectofotometru). Cantitatea de antigen sau anticorp, din proba de testat, este proportionala cu cantitatea de conjugat legata. Sub actiunea enzimei din conjugat, substratul adaugat se coloreaza, iar intensitatea culorii citita colorimetric, se exprima ca densitate optica (DO). Pentru evaluarea rezultatelor, se determina, in prealabil, curba standard a valorilor obtinute, prin testarea antigenului sau anticorpului, in concentratii cunoscute.
Tehnica indirecta (pentru decelarea anticorpilor):
- absorbtia antigenului pe suport solid;
- introducerea serului de testat si cuplarea anticorpului cu antigenul fixat;
- introducerea conjugatului imunoglobulinicantispecie-enzima (specia de la care provine anticorpul) si cuplarea acestuia cu complexul antigen-anticorp;
- evidentierea enzimei fixate cu ajutorul unui substrat specific enzimei din conjugat.
Tehnica directa (pentru detectarea antigenelor):
- se absoarbe anticorpul pe substratul solid;
- se introduce antigenul din proba de examinat, care se cupleaza cu anticorpul fixat pe suport;
- se introduce conjugatul anticorp-enzima specific antigenului;
- se evidentiaza enzima fixata, cu ajutorul unui substrat specific enzimei de conjugat.
Tehnica dublu anticorp (sandwich) pentru decelarea antigenelor:
- se absoarbe anticorpul pe suportul solid;
- se introduce antigenul din proba de examinat, care se cupleaza cu anticorpul fixat;
- se introduce anticorpul specific antigenului din proba de examinat (preparat pe alta specie decat specia de la care provine primul anticorp fixat pe suport);
- se adauga conjugatul imunoglobulina antispecieenzima (preparat pe aceeasi specie, pe care a fost preparat al doilea anticorp specific antigenului)
- se introduce substratul pentru evidentierea enzimei fixate.
Trusa de diagnostic ELISA, rapid polivalenta, este destinata si pentru determinarea anticorpilor serici la om si la animale fata de Trichinella spiralis.
Reactivii si modul de utilizare al setului ELISA, permite realizarea reactiei in 20 de minute, la temperatura camerei, folosind materiale si recipienti din dotarea trusei. Interpretarea reactiei la probele de testat, se face cu ochiul liber, prin atie, in functie de culoarea probelor martor: etalon pozitiv, slab pozitiv si negativ.
Testul imuno-enzimatic ELISA este de 100010.000 de ori mai sensibil decat testul trichineloscopic al probelor de muschi, prelevate din diferite regiuni anatomice de electie, care evidentiaza prezenta parazitului dupa 2030 de zile de la infectare.
Setul de diagnostic ELISA rapid, care foloseste antigen purificat excretor-secretor (ES), preparat din larvele de Trichinella spiralis, este specific si sensibil.
Principiul metodei: in timpul primei incubari, anticorpii din serul de cercetat, se cupleaza cu antigenul din godeul de reactie. Urmatoarea incubatie permite legarea conjugatului Proteina APeroxidaza de complexul anticorp-antigen. Dupa spalarea conjugatului necuplat, se adauga un substrat care produce schimbarea culorii in albastru, in prezenta complexului enzimatic si a peroxidului.
Solutia de stopare, opreste reactia si transforma culoarea albastra in galben. In godeurile de reactie, unde nu exista proteina APeroxidaza cuplata la complexul antigenanticorp, reactia este incolora. Acest test detecteaza in primul rand anticorpii de tip IgG, datorita utilizarii de Proteina A, drept conjugat enzimatic.
Limitele testului: la om, rezultatele serologice trebuie utilizate prin coroborare cu datele clinice, epidemiologice si biochimice. Rezultatele negative vor fi retestate dupa trei saptamani, deoarece nivelul anticorpilor ar fi putut fi sub nivelul de detectare. Numarul indivizilor prezentand rezultate pozitive, poate varia semnificativ, in functie de populatie si zona geografica.
Testele serologice devin pozitive, dupa trei saptamani de la infestare si au persistenta de cativa ani; experimental, a fost stabilit urmatorul procent de rezultate pozitive ELISA, pe probe recoltate de la pacienti infectati (confirmati prin biopsie), in functie de dinamica anticorpilor, determinata de timpul scurs din momentul infectarii:
|
Saptamani post-infestare |
3 |
5 |
7 |
15 |
57 |
|
% |
25 |
94 |
100 |
100 |
57 |
In cazurile de infectare mai redusa (nu putine in practica), rezultatul examinarii prin ELISA va fi negativ. Avem de-a face cu reactii fals negative, care pot fi cauzate, pe langa o doza infectanta redusa si de o depresie imunitara. Mai putin importante, sunt reactiile fals pozitive, cauzate de prezenta unor anticorpi indreptati impotriva altor helminti si protozoare.
Pentru sensibilitatea testului imuno-diagnostic, o importanta deosebita o prezinta antigenele folosite. Trichinella prezinta, nu numai un mare numar de fractiuni antigenice, dar si o dinamica accentuata si un mimetism impresionant pentru fiecare stadiu de dezvoltare. Astfel, larvele de Trichinella spiralis L1, au la suprafata patru antigene diferite, cu diverse greutati moleculare: 28, 30, 58, 64 KD.
Dintre acestea, de exemplu, cea de 64 KD se identifica prin imunofluorescenta cu anticorpi monoclonali numai pana la varsta de opt ore a larvelor. In productia de antigene cu TSL1 in vitro, este important a se prepara antigenele in culturi sub 24 de ore (short time cultures). Antigenele preparate prin cultivare mai indelungata cresc substantial rata reactiilor fals pozitive.
Ca tendinte actuale, mentionam inlocuirea omogenatelor parazitare (predispuse la reactii incrucisate fals pozitive), cu antigene specifice glicoproteice secretate de larve in medii sintetice de cultura, sau obtinute prin inginerie genetica (grefarea genei parazitare corespunzatoare pe E. coli).
Imunoblotul (Western Blot)
Recunoasterea antigenului muscularlarvar de diverse tipuri de Trichinella (T1T8), este preferabila in etapa initiala de identificare, prin recunoasterea raspunsului la extrasul total solubil de muschi larvar prin Western Blot. Moleculele antigenice, care au fost cel mai constant recunoscute, aveau mase moleculare (MM) de 96, 67, 63, 60, 55 si 47 KDa. Prin izolare pe gel de poliacrilamida, s-au mai evidentiat doua produse de 43 si 47 KDa, care purificate, au dat cele mai sensibile si specifice rezultate la ELISA (42). Si alti autori considera Western Blot-ul util, atunci cand se doreste evaluarea specificitatii de specie (de pilda intre Trichinella spiralis nativa si britovi) [38]. Antigenul polipeptidic ES este recunoscut la W. B.
O investigatie ampla a serurilor pacientilor cu trichineloza, efectuata prin WesternBlot la departamentul de imunologie al Institutului National de Diagnostic si Epidemiologie din Mexic a plecat de la extrasul crud de Trichinella spiralis ca si context antigenic. S-au obtinut 8 bande distincte cuprinse intre 38 104 KDa la marea majoritate a pacientilor, raspunsul seric fiind destul de omogen.
O buna parte din benzile caracteristice obtinute la W. B., au fost recunoscute si de serurile unor rozatoare infestate si de iepuri imunizati si in a doua etapa a studiului, au fost recunoscute de anticorpi monoclonali si policlonali fata de Trichinella spiralis, proveniti de la sobolani, soareci, porci si iepuri infestati sau imunizati cu Trichinella spiralis.
Datele obtinute indica astfel ca, diverse specii animale, la fel ca si oamenii, recunosc o categorie comuna de epitopi (determinanti imuni) imunomodulati de Trichinella spiralis.
Testul imuno enzimo chemoluminescent (Enzyime chemolumines-cent immunoassay)
S-a dovedit deosebit de eficient si practic, in detectarea anticorpilor sub forma de screening, in masa, al porcilor in abatoare. Necesita 45 de minute, metodologia este simpla, iar indicele de pozitivitate este abil cu cel obtinut prin ELISA efectuata cu antigen de tip IgG. Dezavantajul consta in pretul ridicat al suportului magnetic.
Tehnicile de amplificare ADN
Metoda de amplificare a acidului dezoxiribonucleic (Random amplified polymorphic DNARAPD) reprezinta cea mai sensibila procedura pentru a face diferentierea intre diversele poluri genetice de Trichinella, si se aplica frecvent pentru identificarea speciilor de Trichinella spiralis si Trichinella britovi.
Etapele tehnice sunt urmatoarele: larvele sunt recoltate din carne proaspata sau congelata si se stocheaza la -20C timp de o luna, sau in alcool etilic 70%, timp de 30 de zile, la temperatura camerei. Hibridizarea ADN s-a folosit, cu succes, pentru evidentierea Trichinellei pseudospiralis la specii animale la care nu era inca identificata. De asemenea, repetitiv-replicarea ADN a evidentiat heterogenitati chiar si in cadrul aceluiasi pol genetic. Profilul ADN repetitiv se stabileste cu ajutorul endonucleazelor.
Formele usoare de boala nu necesita izolare obligatorie in spital. Formele medii si severe se spitalizeaza. Se pastreaza repausul la pat, pe toata durata manifestarilor acute. Dieta este hipercalorica cu un aport suplimentar de calciu, potasiu, proteine.
Gradul de reusita al tratamentului este intr-o buna masura invers proportional cu durata cuprinsa intre momentul infestarii si cel al aplicarii tratamentului. Cu cat tratamentul se aplica mai timpuriu, cu atat rezultatele sunt mai bune. Se accepta limita de 30 de zile pentru o reusita terapeutica sigura. Pe masura inaintarii in timp (dupa 45 saptamani post infectare), lucrurile incep sa se complice, din cauza intrarii larvelor sub protectia membranelor chistice.
Scopul terapiei stadiilor precoce ale infectiei este de a limita invazia musculara a larvelor, atunci cand aceasta s-a produs deja, de a reduce distrugerea tesutului muscular, care e responsabil pentru majoritatea manifestarilor clinice.
Masurile terapeutice sunt specifice, in functie de faza evolutiva a parazitului. In faza intestinala, se administreaza Mebendazol 200 400 mg x 3/zi timp de 7‑10 zile sau Albendazol: 1015 mg/kgc/zi timp de 7 zile. Terapie adjuvanta: calciu per os, antispastice intestinale.
In faza circulatorie, formele severe reprezinta urgente medicale, prin riscul alergodermiilor de tip angioedem, terapia patogenica devansand-o pe cea antiparazitara. Se administreaza steroizi: prednison 1 mg / kgc/ zi 1014 zile. In formele usoare: AINS. Terapia antiparazitara se face cu Albendazol 1015 mg/kgc/zi timp de 10-l4 zile. Ca alternative, se administreaza Thiabendazol (Mintezol) 50 mg /kgc /zi in 2 prize, timp de 7 10 zile. Ca terapie adjuvanta, se administreaza antitermice, solutii perfuzabile cu glucoza. In faza musculara, daca pacientul prezinta mialgii, curbatura, oboseala cronica, se administreaza Albendazol 1015 mg / kgc/ zi timp de 10 zile si terapie adjuvanta: AINS, miorelaxante, calciu per os. Rezultate bune se obtin si dupa administrarea de dietilcarbamazepina (Loxuran) 6 mg/zi timp de 10 zile. Poate fi utilizata si in fazele mai avansate ale bolii, deoarece patrunde mai bine in chisturi.
Antihelminticele: Albendazol, Mebendazol si Thiabendazol reprezinta medicatia antihelmintica in uz la ora actuala. Aceste medicamente actioneaza prin legarea betatubulinei parazitului, care impiedica asamblarea microtubulilor si inhiba transportul de glucoza, rezultand imobilizarea si moartea parazitului.
Albendazolul scade productia de ATP, cauzand depletie de energie, imobilizarea si moartea parazitului. Pentru a evita raspunsul inflamator la nivelul SNC, se administreaza impreuna cu anticonvulsivante si glucocorticoizi. Este practic insolubil in apa. Absorbtia e imbunatatita dupa o masa bogata in grasimi. Absorbtia e buna la nivelul SNC si toleranta mai buna decat thiabendazolul.
Posologia depinde de greutatea corporala a pacientului si severitatea infectiei. Dozele uzuale sunt cuprinse intre 400 si 800 mg/zi timp de 5-30 zile. Ciclul terapeutic se poate repeta dupa o pauza de 14 zile.
Contraindicatii: In caz de hipersensibilitate la constituentii produsului, in sarcina sau la femeile presupuse a fi insarcinate.
Interactiuni medicamentoase: coadministrarea carbamazepinei ii poate reduce eficienta; dexametazona ii poate creste toxicitatea, cimetidina ii creste concentratia, nu s‑au observat interactiuni cu teofilina.
Reactii adverse: cresterea nivelului enzimelor hepatice, tulburari digestive, leucopenie, vertij, cefalee, alopecie reversibila si febra; rar, pancitopenie si reactii de hipersensibilitate (rash, prurit, urticarie).
Daca nivelul enzimelor hepatice creste semnificativ, tratamentul trebuie intrerupt. Inaintea fiecarui ciclu de tratament si cel putin din doua in doua saptamani, in cursul tratamentului, trebuie efectuate teste functionale hepatice.
Proba pe om a Albendazolului a fost facuta, initial, in cadrul unei epidemii de trichineloza prin ingestie de carne de cal, in decembrie 1993, in Franta, cand s‑au inregistrat 500 de cazuri. S-a at eficienta imediata si pe termen mediu, precum si toleranta terapiei cu Thiabendazol si Albendazol la 46 de pacienti, care au primit concomitent si Prednison.
Rezultatele se pot sintetiza astfel: la tratamentul cu Thiabendazol, recaderile (reacutizarile) au aparut in raport de 7/1 fata de Albendazol, iar efectele secundare s-au notat numai la 7 pacienti, toti tratati cu Thiabendazol. La 6 luni, pacientii chestionati au reclamat ca simptome: mialgii (81%) si fatigabilitate (69%), fara diferente semnificative intre cele doua grupe. Per ansamblu, se poate admite superioritatea terapeutica a Albendazolului.
Mebendazolul determina moartea parazitului prin blocarea selectiva si ireversibila a transportului de glucoza si alti nutrienti din intestin.
Contraindicatii: hipersensibilitate la Mebendazol, sarcina si alaptare. Interactiuni medicamentoase: carbamazepina si fenitoina ii pot scadea efectele; cimetidina ii poate creste concentratia.
Reactii adverse: dureri abdominale tranzitorii si diaree, in timpul terapiei initiale, in infectiile masive (se remit dupa cateva zile de terapie); reactiile rare includ: leucopenie, agranulocitoza, hipospermie.
Thiabendazolul (Mintezol) se utilizeaza in infectiile helmintice mixte; inhiba fumarat reductaza mitocondriala specific helmintica; amelioreaza simptomatologia trichinelozei in timpul fazei de invazie. Prezinta valoare redusa in cadrul fazelor tardive ale bolii. Folosirea sa e limitata de efectele adverse frecvente. E disponibil in tablete de 500 mg si suspensie 500 mg/5 ml. Se administreaza in timpul meselor.
Doza la adulti: 50 mg/kg/doza p.o. 5 doze.
Contraindicatii: hipersensibilitate la produs.
Interactiuni medicamentoase: poate creste nivelul teofilinemiei, inducand toxicitate.
Sarcina: nu s-a demonstrat ca este sigura administrarea in timpul sarcinii.
Reactiile adverse pot aparea la aproximativ 50% din pacienti. Acestia experimenteaza unul sau mai multe efecte adverse, incluzand: greata, varsaturi, anorexie, cefalee, prurit, vertij. Ocazional se pot constata leucopenie, rash, halucinatii si alte manifestari psihiatrice, tulburari vizuale si olfactive, eritem multiform; reactii rare includ: soc, tinitus, colestaza intrahepatica, convulsii, edem angioneurotic, sindrom StevenJohnson. Nu se administreaza imediat inaintea activitatilor care necesita vigilenta. Se monitorizeaza atent pacientul, in cazul disfunctiilor hepatice sau renale; inainte de initierea terapiei, se corecteaza anemia si deshidratarea. Se foloseste in infectiile parazitare confirmate, nu profilactic.
Eficacitatea tratamentului se evidentiaza prin ameliorarea simptomatologiei pacientului.
Corticoterapia se administreaza in infectii severe, cu semne de soc, sau interesare severa cardiaca, pulmonara sau nervoasa. Imunosupresia, datorata corticoterapiei, desi de multe ori salvatoare, prelungeste viata parazitilor in tractul gastrointestinal, ceea ce duce la cresterea producerii de larve.
Se administreaza Prednison 1 mg/kgc/zi, cu reducerea progresiva a dozelor. Desi majoritatea autorilor recomanda doze moderat crescute de corticoizi, in tratamentul trichinelozei, in cazurile severe, pot fi necesare doze crescute.
Nu exista contraindicatii absolute ale glucocorticoizilor atunci cand administrarea acestora este de importanta vitala. Atunci cand riscurile depasesc beneficiile, nu se administreaza la pacientii care prezinta: ulcer gastroduodenal, osteoporoza, psihoze, herpes, varicela, zona zoster.
La intreruperea brusca a dozelor, apar fenomene de insuficienta a CSR. Printre efectele secundare ale corticoterapiei se numara: hiperglicemie, osteonecroza, miopatie, ulcer peptic, hipokaliemie, osteoporoza, euforie, psihoze, miastenia gravis, intreruperea cresterii, infectii.
Ciclosporina A s-a experimentat la soarecii infestati cu 200 larve de Trichinella spiralis; ei au primit intraperitoneal Ciclosporina, 50mg/kg/zi, intre zilele 1418 post‑infectie. La animalele tratate, reactiile parazitare induse au fost mai putin intense. In plus, stimularea populatiei limfocitare LCD8+, in special in jejun, a fost mai puternica, ceea ce este important, deoarece LCD8+ au efect citotoxic antiparazitar. Alte investigatii au aratat ca in trichineloza experimentala, Ciclosporina A actioneaza asupra larvelor, atat in vitro, cat si in vivo, diminuand numarul acestora si intensitatea reactiilor celulare. Eficacitatea este insa dependenta net de precocitatea administrarii.
Levamisolul, administrat mai mult ca imunostimulant, a determinat in trichineloza experimentala, la examenul in M. E., formarea accelerata a chistelor pe suprafata diafragmului; efectul lor a fost direct proportional cu precocitatea administrarii sub 6 zile.
Alte investigatii privind Levamisolul, se refera la raspunsul inflamator si imun al gazdei. S-a demonstrat astfel ca, administrarea precoce redreseaza raspunsul imun, prin hipersensibilitate de tip intarziat, care este diminuata de infectie si creste depunerea de colagen in jurul larvelor. Poate fi acceptat, deci, ca tratament adjuvant.
Cromoglicatul de sodiu a fost experimentat la soarece, dupa infestarea cu 200 larve de Trichinella spiralis. Tratamentul s-a efectuat in doze de 0,6 sau 1,7mg/soarece/zi. S-a evidentiat un numar mai mare de mastocite si eozinofile, in atie cu martorii. Se poate deci admite efectul adjuvant al cromoglicatului.
Asociatia corticoizi - ciclofosfamida a fost experimentata in etapa musculara a trichinelozei la sobolan, inainte si dupa incapsulare. S-au efectuat sectiuni colorate cu hematoxilina ‑ eozina, pentru evidentierea modificarilor histologice si testul imunoperoxidazic, pentru evaluarea locala a antigenului parazitar. Efectele au fost favorabile, cu conditia administrarii asociatiei inainte de inchistarea completa.
Interferonul gama s‑a administrat intraperitoneal la soarecii infestati cu Trichinella spiralis, cate 10 U IFN, timp de 7 zile, incepand cu ziua 14 postinfectie. S‑au recoltat probe de muschi striat (diafragm) la 4, 8 si 12 saptamani si s-a studiat: gradul de incarcatura larvara, gradul de inchistare si de digestie a larvelor. Paralel, s-au efectuat studii imunohistochimice ale celulelor inflamatorii din jurul larvelor inchistate. Se constata ca IFN gama influenteaza, in sens favorabil, subseturile limfocitelor CD4+ si CD8+, dar nu induce diferente semnificative privind gradul de inchistare, digestie sau incapsulare, la area cu martorii.
Fexofenadina suprima atat eozinofilia, cat si anafilaxia sistemica, care sunt reactii fundamentale in bolile alergice. La soarecii C57BL/6, administrarea orala, repetata de fexofenadine HCl (5,10 si 20 mg/kg/zi) a determinat suprimarea eozinofiliei dependenta de doza. Aceasta nu s-a observat la soarecii W/W (v) deficienti in celule mastocitare. In plus, administrarea orala unica de fexofenadine HCl (10 si 20 mg/kg) suprima, semnificativ, scaderea temperaturii rectale, un marker utilizat pentru anafilaxia sistemica la soarecii C57BL/6. La soarecii CBF1, injectati cu ser de la soarecii NC/Nga cu niveluri ridicate de IgE, scaderea temperaturii rectale a fost suprimata de administrarea in doza unica de fexofenadine HCl (10 si 20 mg / kg). Fexofenadina nu a avut efect asupra nivelurilor periferice de IL-5 si eotoxina.
Imunizarea soarecilor cu antigen excreto-secretor induce protectie si modificarea subtipurilor limfocitare. Protectia si raspunsul imun au fost studiate la soarecii imunizati cu antigen excreto-secretor de Trichinella spiralis (ES Ag), fara adjuvant. Astfel, imunizarea cu ES Ag a produs rate inalte de protectie impotriva stadiilor adulte (98,4%) si larvelor musculare (82,9%). Au predominat citokinele de tip Th2 (IL -l0, IL 4). ES Ag a fost semnificativ crescut in ordinea Ig G2a > Ig G1 >IgG, a doua zi dupa imunizarea finala si in ziua a 7-a dupa infestarea experimentala cu larve vii de Trichinella spiralis.
Expresia LCD4+ si a raportului LCD4+/CD8+ din splina si sange au fost semnificativ crescute. Aceste rezultate demonstreaza ca imunizarea cu antigen de Trichinella spiralis induce un raspuns imun robust determinand protectia completa impotriva larvelor infectante, aceasta protectie putand fi atinsa fara utilizarea vreunui adjuvant.
Masura profilactica majora este reprezentata de educatia sanitar-veterinara. Nici un specialist si nici o medicina veterinara sau umana, oricat ar fi de performanta, nu vor putea sa suplineasca actiunea constienta a proprietarilor si ingrijitorilor de animale, a celor ce prelucreaza si comercializeaza carnea si produsele din carne, a consumatorilor de carne. In arealul nostru, individul trebuie sa inteleaga ca, invazia de Trichinella vine catre el, in mod special de la porc, prin carnea parazitata a acestuia.
Prin actiunile sale, omul poate stopa ofensiva Trichinellei, aparandu‑se, atat pe el si pe ai lui, cat si animalele. Daca animalelor nu li se administreaza, de catre om, in hrana, deseuri culinare ce pot fi infestate cu larve de Trichinella, supe proteice insuficient prelucrate termic, cadavre si altele, acestea vor ramane neparazitate si nu vor prezenta pericol de infectare pentru om.
Daca omul, proprietar, administrator sau ingrijitor de animale, nu va introduce in efectivul sau de animale, porcine provenind din mediu infestat si daca va asigura conditii normale de furaje, cazare si zooigiena care sa previna tulburarile de metabolism si consecintele acestora canibalismul - atunci animalele vor ramane sanatoase si carnea lor nu va prezenta un pericol.
Cand individul este pus in situatia de a procura si consuma carne de porc sau de vanat, din comert sau din alte surse, omul poate sa previna infestarea, prin actiunea sa constienta in momentul procurarii, evitand sa accepte un produs cu origine necunoscuta sau necontrolat sanitar veterinar.
Hotararea de guvern nr. 524 din 8 august 1994, privind aprobarea Programului National de supraveghere, prevenire si combatere a trichinelozei, stipuleaza urmatoarele masuri, pentru prevenirea infectiei cu Trichinella spiralis la om:
1. Pentru prevenirea imbolnavirilor, inainte de a fi data in consum, se executa in mod obligatoriu, examenul pentru trichineloza, la carnea provenita din taierea animalelor receptive la aceasta boala (porcine, mistreti, cai, nutrii)
2. Carnea examinata si gasita fara Trichinella spiralis, se marcheaza cu o stampila dreptunghiulara cu inscriptia Fara trichina, aplicata pe fata externa a pulpei, si se da in consum proaspata sau la preparate din carne.
3. Se interzice darea in consum a carnii, organelor si subproduselor provenite de la animale infectate cu Trichinella spiralis, care vor fi distruse prin ardere sau denaturare si ingropare sub directa supraveghere si raspundere a organelor sanitar-veterinare.
4. In cazul aparitiei de imbolnaviri de trichineloza, Directia Sanitara Veterinara, impreuna cu Inspectoratul de Politie Sanitara si Medicina Preventiva Judetean, vor efectua ancheta epidemiologica, pentru a stabili originea carnii sau preparatelor din carne, care au determinat imbolnavirile si gradul de infectie existent in zona respectiva, atat la oameni, cat si la animale, conform prevederilor Ordinului comun nr. 25/474/1993 al ministrului agriculturii si alimentatiei si al ministrului sanatatii.
5. Raportarea cazurilor de trichineloza confirmata la om este obligatorie si se face conform instructiunilor Ministerului Sanatatii
6. Se vor intensifica actiunile de informare si educare a populatiei, insistandu-se asupra necesitatii controlului sanitar-veterinar si asupra prelucrarii termice corecte a carnii.
Distrugerea (inactivarea sau devitalizarea) larvelor de Trichinella din carne si produse din carne, se poate realiza cu ajutorul caldurii, frigului si iradierii; eficacitatea este dependenta de intensitatea agentului fizic, de grosimea bucatilor de carne si de durata de expunere.
Distrugerea prin fierbere. Carnurile slab infestate si fara modificari patologice, sectionate in bucati de pana la 8 cm grosime se fierb in vase bine acoperite timp de 2 ore. Preparatele culinare obisnuite: prajeli, fripturi la gratar, carne la cuptor, nu omoara toate larvele situate in profunzimea bucatilor de carne si pun in pericol sanatatea consumatorilor neavizati.
Distrugerea larvelor prin frig (congelare, inghetare) se realizeaza la -l5C timp de 20 de zile, la -23C timp de 10 zile, la -29C timp de 6 zile (bucatile de carne trebuie sa aiba diametrul de cel mult 15 cm).
Respectarea masurilor de profilaxie si a dispozitiilor legale conduc la reducerea incidentei si prevalentei trichinelozei din arealul nostru geografic.
DATE GENERALE Trichineloza este boala produsa de prezenta helminlului Trichinella spiralis. in stadiul adult, parazitul are o forma cilindro-conica [...] |
a) Agentul etiologic. Este un parazit, trichina sau trichinela (Trichinella spiralis), din clasa nematodelor. Adultul ca mascul, masoara in lungime 1, [...] |
Pulmonul nu rainine indiferent in fata unor afectiuni de durata, insotite de tulburari grave metabolice sau de sistem. Este vorba de unele p [...] |
Copyright © 2010 - 2025
: eSanatos.com - Reproducerea, chiar si partiala, a materialelor de pe acest site este interzisa!
Informatiile medicale au scop informativ si educational. Ele nu pot inlocui consultul medicului si nici diagnosticul stabilit in urma investigatiilor si analizelor medicale la un medic specialist.
Termeni si conditii - Confidentialitatea datelor - Contact