REACTIA SISTEMICA POSTAGRESIVA
(Raspunsul neurohormonal, metabolic, imunologic si celular la agresiune)
1. Introducere
Organismul uman supravietuieste in mediul inconjurator datorita mentinerii unui echilibru dinamic, extrem de complex si armonios denumit de Cannon in l939 homeostazie.
In lumina cunostintelor actuale denumirea de stabilitate homeodinamica pare a fi mai adecvata deoarece sugereaza mai bine caracterul dinamic care reprezinta esenta acestui fenomen.
Stabilitatea homeodinamica este supusa permanent unor tendinte la modificare de catre forte perturbatoare intrinseci sau extrinseci denumite stresori sau agenti agresori.
In sens larg stresul poate fi, asadar, definit ca o stare de dizarmonie sau amenintare a stabilitatii homeodinamice. Raspunsul adaptativ la stres poate fi specific unui stresor (agent agresor) sau poate fi generalizat si nespecific. Raspunsul generalizat si nespecific 212b14c este stereotip si apare, in general, numai daca amploarea amenintarii asupra homeostaziei depaseste anumite limite.
In decursul timpului, modificarile adaptative provocate de
agentii agresori au purtat diferite denumiri :'Maladie
postoperatoire' -
Atat traumele accidentale cat si interventiile chirurgicale elective sunt identice in amenitarea fiziopatologica pe care o reprezinta.
Cu toate ca agresiunile sunt diferite de la un pacient la altul, ca mod de instalare, numar de organe implicate si amploare , raspunsul biologic este similar.
Stresorii (agentii agresori) fizici sau emotionali declanseaza raspunsuri centrale si periferice desfasurate in scopul mentinerii stabilitatii homeodinamice.
In prezenta unor agresiuni majore traumatice, infectioase, sau a inanitiei, amenintarea asupra stabilitatii homeodinamice este de amploare crescuta, determinand aparitia unui raspuns stereotip, generalizat si nespecific 212b14c avand ca scop restabilirea stabilitaitii cardiovasculare, mentinerea aportului tisular de oxigen, mobilizarea de substrat energetic, vindecarea plagii si minimalizarea durerii.
Raspunsul adaptativ optim depinde nu numai de capacitatea de a raspunde rapid la stimuli, ci in egala masura de abilitatea de a activa elementele contrareglatoare care impiedica un raspuns exagerat. Fara controlul acestor elemente restrictive raspunsul la agresiune isi pierde calitatea adaptativa si poate produce modificari patologice severe.
Una din cele mai dificile probleme cu care se confrunta medicul reanimator este diferentierea unei reactii adaptative benefice de una exagerata, prin definirea punctului in care un raspuns pozitiv cu efecte favorabile devine o autoagresiune.
In practica se considera ca reactia exagerata de raspuns a organismului apare atunci cand agresiunea este de asemenea amploare incat supravietuirea este imposibila fara interventie medicala.
Aceasta realitate poate fi ilustrata prin cateva exemple. in situatia in care o persoana tanara care a suferit un traumatism sever cu fractura de femur si pelvis este tratata conservator, exista un mare pericol de moarte sau in cel mai bun caz vindecarea este de foarte lunga durata. Daca in aceiasi situatie este aplicat un tratament chirurgical adecvat sub anestezie si terapie intensiva moderna, raspunsul organismului va fi aproape nedetectabil, iar vindecarea se produce intr-un timp semnificativ mai scurt.
Un alt exemplu este reprezentat de un pacient traumatizat care a pierdut o parte din volumul sanguin. Daca restabilirea volumului circulant si tratamentul chirurgical sunt aplicate imediat sistemele de aparare nu au posibilitatea sa actioneze exagerat si distructiv. Cantitatea maxima de sange pe care un individ poate tolera sa o piarda fara interventie medicala se situeaza probabil undeva intre 1000 si 1500ml si este aproape imposibil ca cineva sa supravietuiasca la pierderea unor cantitati mai mari de sange fara repletie volemica adecvata.
Infectia poate constitui un alt exemplu. Este evident faptul ca simpla prezenta a germenilor microbieni in sangele circulant (bacteriemie, viremie etc.) nu este periculoasa. Germenii microbieni devin periculosi din cauza eliberarii unor substante toxice care activeaza sistemele de aparare ale organismului, care la randul lor, in anumite conditii, pot distruge nu numai germenul dar si o parte a masei celulare normale a organismului.
Toate aceste observatii atesta realitatea unanim acceptata in prezent ca numai cunoasterea tuturor aspectelor raspunsului la agresiune si aplicarea in timp util a mijloacelor moderne de terapie intensiva permite supravietuirea pacientilor cu boli extrem de severe, sau efectuarea cu succes a unor interventii chirurgicale extensive.
2. Semnalele aferente ale reflexului la agresiune:
Injuria determina alterari ale echilibrului homeodinamic percepute de catre receptori si transformate in semnale aferente (input) ce sunt transmise pe cai specifice sistemului nervos central. Aici sunt integrate si prelucrate si determina producerea unui complex de semnale eferente (output) ce stimuleaza sau inhiba efectorii neuroendocrini ce produc modificari fiziologice in scopul corectarii perturbarilor homeodinamice (. 1).
Stimulii actioneaza asupra unor receptori specializati ce ii pot transforma in impuls nervos si informatia va fi astfel transmisa spre sistemul nervos central.
Stimulii primari ai reflexelor neuro-endocrine sunt:
2.1. Modificarile volumului sanguin circulant efectiv
Aproape toate injuriile sunt caracterizate prin scaderea volumului sanguin circulant efectiv(VSCE). Hemoragia, sechestrarea de volum plasmatic (ca in deshidratare, pierderi in spatiul trei, sau arsuri) si inabilitatea sangelui de a circula (ca in insuficienta cardiaca, tamponada sau embolie pulmonara ) sunt scenarii tipice pentru acest stimul.
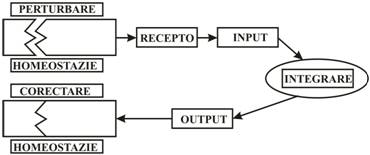
.1. Reactia la agresiune - Raspuns nespecific, generalizat.
Scaderea VSCE este sesizata de baroreceptorii de joasa presiune din atrii, influentati de modificarile volumului atrial si de baroreceptorii de inalta presiune localizati in aorta, arterele carotide si arterele renale sensibili la modificarile de presiune arteriala.
VSCE si volumul sanguin total nu sunt identice, volumul circulant total devenind efectiv numai daca este sesizat de acesti receptori. De aceea insuficienta de pompa sau sechestrarea de lichide in spatele unei obstructii (pneumotorax in tensiune, tamponada cardiaca, ciroza) determina un VSCE mai mic decat volumul circulant total. Chiar si atunci cand volumul circulant total este crescut, ca in insuficienta cardiaca, VSCE sesizat de receptorii de joasa si inalta presiune este scazut, ceea ce determina mentinerea retentiei de apa si sare si a rezistentei vasculare crescute.
Scaderea VSCE determina reducerea activitatii baroreceptorilor manifestata prin pierderea inhibitiei tonice. Semnalele aferente dela baroreceptori produc inhibitie tonica asupra eliberarii mai multor hormoni asupra osului" class="text">hormoni si induc activarea sistemului nervos central si a sistemului nervos vegetativ.. Aferentele de la baroreceptori sunt transmise prin nervul vag, prin tractusul solitaris al bulbului si formatia reticulata a trunchiului si hipotalmusului. Reducerea activitatii baroreceptorilor determina stimulare neuroendocrina, care include secretia de angiotensina II (AII), via renina, secretia de aldosteron via AII si ACTH, secretia de glucagon via epinefrina si reducerea secretieiei de insulina prin efect epinefrinic.
Scaderea VSCE sesizata de baroceptorii de la nivelul aparatului juxtaglomerular renal determina deasemenea secretia de renina si formarea ulterioara de angiotensina si secretia de aldosteron.
Pierderea inhibitiei tonice a baroreceptorilor mediaza deasemenea stimularea ritmului cardiac, cresterea contractilitatii miocardice si vasoconstrictie prin cresterea activitatii simpatice si scaderea activitatii parasimpatice.
Raspunsurile neuro-endocrin si vegetativ initiate de scaderea VSCE sunt proportionale cu marimea deficitului. Raspunsul este mai mare la o pierdere de 20% din VSCE decat la o pierdere de 10%. Raspunsurile neuro-endocrine si cardio-vasculare au un maxim de efect compensator la o pierdere de volum sanguin de 30-40%. Scaderea ulterioara a volumului sanguin nu mai poate fi compensata si apare hipotensiunea arteriala.
2.2. Modificarile concentratiilor de oxigen, bioxid de carbon si a ionilor de hidrogen
Chemoreceptorii periferici sunt formatiuni de 1-2 mm compuse din tesut bine vascularizat ( celule glomus) cu continut dopaminergic, ce sunt localizate la nivelul glomusului carotidian (receptori primari ) si la nivelul arcului aortic.
in mod normal acesti receptori nu sunt activati. Celulele glomusului carotidian sunt activate in principal de reducerea concentratiei de oxigen si in mai mica masura de cresterea presiunii partiale a CO2 si de cresterea concentratiei ionilor de hidrogen. Chemoreceptorii raspund cel mai rapid la o presiune partiala a oxigenului mai mica de 50 mmHg.
Activarea chemoreceptorilor produce o stimulare a hipotalamusului si a componenetei vasculare a sistemului vegetativ simpatic, ce determina tahicardie si cresterea contractilitatii miocardice.
Cei mai importanti chemoreceptori centrali sunt situati la nivelul bulbului ventral , sunt inconjurati de lichidul cefalorahidian si sunt sensibili la modificarile PCO2 si pH-lui.
Activarea chemoreceptorilor centrali stimuleaza centrul respirator, producand cresterea ritmului respirator. Hipovolemia este insotita de tahipnee datorita scaderii VSCE care activeaza chemoreceptorii prin reducerea fluxului sanguin.
Activarea chemoreceptorilor produsa de scaderea PaO2 este potentata de hipercapnie si acidemie.
Activarea chemoreceptorilor se produce si de catre prostaglandinele si kininele circulante si determina reflexe complexe mediate de aferentele vagale si simpatice.
2.3. Durerea si stimulii emotionali
Durerea si trairile emotionale sunt caracteristice agresiunii si conduc la activarea sistemului neuro-endocrin.
Durerea actioneaza prin proiectiile fibrelor nociceptive periferice in sistemul nervos central determinand stimularea talamusului si hipotalamusului.
Trairile emotionale sunt produse de perceptia sau pericolul injuriei, care prin intermediul ariilor limbice centrale produc un raspuns emotional manifestat sub forma de furie, teama sau anxietate. Aceste modificari emotionale stimuleaza reflexe neuro-endocrine prin proiectii de la sistemul limbic, hipotalamus si nuclei ai trunchiului cerebral.
Atat durerea cat si trairile emotuionale produc cresterea secretiei de vasopresina, ACTH, opioizi endogeni, catecolamine, cortizol, aldosteron si modificari ale activitatii sitemului nervos vegetativ. in acest fel se explica raspunsul 'ht or flight' descris de Cannon.
Durerea si trairile emotionale sunt elementele care justifica diferenta dintre efectele injuriei produse in stare de constienta si injuria produsa la bolnavul sub anestezie.
Atat durerea cat si trairile emotionale sunt manifestari ce trebuiesc controlate si combatute, deoarece produc reactii distructive la nivelul macroorganismului.
2.4. Modificarile substratului energetic
Modificarile concentratiei de glucoza plasmatica reprezinta alterarea primara a substratului ce activeaza reflexele neuro-endocrine. Concentratia plasmatica de glucoza este sesizata de receptorii localizati in hipotalamus (nucleul ventro-medial) si pancreas.
Scaderea concentratiei de glucoza plasmatica stimuleaza eliberarea de catecolamine, hormon somatotrop, cortizol, ACTH, betaendorfina si vasopresina prin cai centrale (hipotalamus si sistem nervos vegetativ) si stimuleaza eliberarea de glucagon prin ambele cai, centrala (hipotalamus si sistem nervos vegetativ) si periferica (activarea directa pancreatica). in acelasi timp secretia de insulina este inhibata pe cale centrala (sistem nervos vegetativ) si de catre pancreas insusi.
2.5. Temperatura
Modificarile temperaturii centrale sunt sesizate in aria preoptica a hipotatamusului si conduc la modificarea secretiei mai multor hormoni: ACTH, cortizol, adrenalina, hormon somatotrop, aldosteron, tiroxina.
Temperatura centrala se poate modifica in urma schimbarii temperaturii mediului ambiant ca rezultat al pierderii integritatii barierei termale tegumentare (arsuri), ca rezultat al scaderii fluxului sanguin hepatic (hipovolemie), sau ca urmare a vasoconstrictiei (hipovolemie) sau vasodilatatiei (sepsis) periferice. Modificarile temperaturii ambiante stimuleaza reflexele neuro-endocrine fie direct, fie prin modificarea temperaturii centrale.
2. Infectia
Infectia reprezinta un stimul puternic al refexelor neuro-endocrine. Prin intermediul endotoxinelor sau exotoxinelor germenii microbieni activeaza initial citokinele proximale pro-inflamatorii (TNF,IL-l, IL-6, IL-8) care la randul lor activeaza celelalte elemente umorale si celulare ale raspunsului inflamator sistemic (sepsis). Prin reteaua complexa de mediatori primari si secundari infectia declanseaza direct sau indirect reflexele neuro-endocrine.
2.7. Plaga
Plaga, chiar si in absenta infectiei, produce o activare a inflamatiei, proces care implica sistemele de aparare ale organismului. Mediatorii eliberati prin activarea sistemului imunitar inflamator (citokine si alti mediatori) au capacitatea sa produca efecte la distanta asupra unor organe si sa declanseze reflexele neuro-endocrine. Marimea plagii este in relatie directa cu dimensiunile manifestarilor raspunsului sistemic al organismului.
3. Integrarea nervos centrala a reflexului la agresiune
Datorita faptului ca raspunsul neuroendocrin la injurie (agresiune) desi indus de mai multe categorii de stimuli, se prezinta remarcabil de constant, s-a presupus ca exista un sistem specific pentru coordonarea sa.
Cele doua componente principale identificate ale Raspunsului general la agresiune sunt: 'corticotropin-releasing hormone' (CRH) si 'locus ceruleus norepinephrine/autonomic (sympathetic) nervous system' (LC/NE sistem simpatic).
Sistemul CRH este larg raspandit la nivel cerebral, dar este cel mai bine reprezentat in nucleul paraventricular (PVN) al hipotalamusului. Sistemul LC/NE simpatic este localizat in trunchiul cerebral. Activarea lui determina eliberarea de noradrenalina dintr-o retea de neuroni cerebrali extrem de densa ducand la cresterea vigilentei si anxietatii.
4. Semnalele eferente ale raspunsului la agresiune
Ramura eferenta a raspunsului reflex la injurie este formata din multiple verigi care pot fi grupate in trei categorii majore de raspunsuri: Raspuns neuroendocrin, Raspuns inflamator (Raspuns al mediatorilor) si Raspuns celular.
Raspunsul neuroendocrin (vegetativ si cel hormonal) sunt generate in regiunile vegetative ale trunchiului cerebral si respectiv axa hipotalamo-hipofizara. Stimulii plecati din aceste regiuni modifica activitatea sistemului nervos vegetativ (SNV), componenta simpatica si parasimpatica si secretia hormonala. Hormonii eliberati pot fi impartiti in hormoni a caror secretie este sub controlul primar hipotalamo-hipofizar (cortizol, tiroxina, hormon somatotrop si vasopresina) si hormoni a caror secretie este sub control primar vegetativ (insulina, glucagon, catecolamine).
Raspunsul inflamator este generat de numeroase peptide mici (factori endoteliali , citokine, autacoizi etc.) eliberate de la nivelul zonei de injurie care au rol local, autocrin sau paracrin. Acest raspuns generat local, capata dimensiuni sistemice datorita actiunilor multiple, la distanta, realizate in special de citokine. Datorita acestui fapt raspunsul poarta in prezent denumirea de 'Raspuns inflamator sistemic'. Mediatorii inflamatori interactioneaza cu hormonii neuroendocrini intr-o maniera complexa care este inca incomplet elucidata.
Raspunsul celular. Pe langa modificarile complexe ce se produc la scara intregului organism stresul induce si o serie de modificari celulare si moleculare care fac parte integranta din raspunsul la agresiune.
4.1. Raspunsul neuroendocrin
Eferenta vegetativa
Stimulii aferenti determina cresterea secretiei hipotalamice de factori de eliberare ( ex. factorul eliberator de corticotropina CRF, peptide intestinale vasoactive VIP). Factorii de eliberare stimuleaza hipofiza, care la randul ei elibereaza: proopiomelanocortina, prolactina, AVP si SH.
CRF actioneaza sinergic cu vasopresina in stimularea secretiei de proopiomelanocortina de la nivelul hipofizei. Proopiomelanocortina este metabolizata in ACTH si beta endorfina, stabilindu-se in acest fel o legatura intre sistemul opioidergic si axul hipotalamo-hipofizar. O alta legatura este realizata de stimularea de catre CRF a eliberarii de catecolamine si enkefaline de la nivelul medularei suprarenale.
S-a demonstrat ca blocarea stimulilor plecati de la nivelul injuriei prin anestezie subarahnoidiana sau anestezie peridurala poate atenua cresterile concentratiilor plasmatice de catecolamine, ACTH, aldosteron, cortizol, renina si AVP.
Dozele mari de morfinice (4 mg/kg morfina, 100microg/kg fentanyl) pot deasemenea diminua cresterea concentratiilor de cortizol si catecolamine, probabil prin suprimarea output-ului de la nivelul sistemului nervos central.
Descoperirea de mediatori neuroendocrini in alte tesuturi decat hipotalamic si hipofizar complica intelegerea fenomenelor complexe ce apar in cadrul reactiei neuroendocrine la agresiune. Astfel, vasopresina a fost identificata la nivelul pancreasului, iar expresia genei de proopiomelanocortina a fost observata in celulele mononucleare periferice, la nivelul splinei, la nivelul rinichiului, la nivelul ovarului si la nivelul plamanului.
Eferenta endocrina
Eferenta endocrina a raspunsului la agresiune este reprezentata de hormoni a caror secretie este sub control primar hipotalamo-hipofizar (cortizol, tiroxina, hormon de crestere) si hormoni a caror secretie se afla sub controlul primar al sistemului nervos vegetativ (catecolamine, insulina, glucagon).
Hormoni sub control hipotalamo-hipofizar
Axul HHS este un sistem dinamic adaptat sa raspunda conditiilor mereu schimbatoare ale organismului si mediului sau (.2). Activitatea axului HHS este reglata printr-un mecanism de feed-back negativ chiar de glucocorticoizi.
Reglarea activitatii axei HHS poate fi impartita in doua categorii: in conditii bazale se face in principal prin nivelul de ACTH si in cazul aparitiei stresului in special prin nivelul cortizolului circulant.
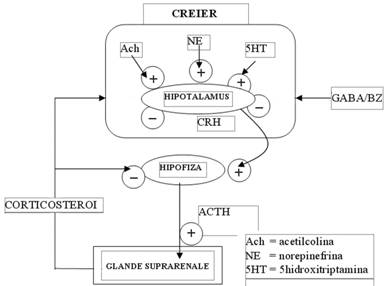
.2. Organizarea si reglarea axului hipotalamo-hipofizo-suprarenal.
CRF, ACTH si Cortizol
Majoritatea tipurilor de agresiune sunt caracterizate prin cresterea secretiei de CRF (factor de eliberare a corticotropinei), ACTH si cortizol care se coreleaza direct cu severitatea agresiunii.
Cresterea eliberarii de ACTH in perioada posttraumatica evolueaza in paralel cu concentratia de cortizol, cu deosebirea ca revenirea la normal a concentratiei de ACTH se face mai rapid, concentratia de cortizol ramanand crescuta o perioada mai lunga de timp.
Cortizolul are actiuni multiple pe metabolismul si utilizarea glucozei, aminoacizilor si acizilor grasi.
La nivel hepatic cortizolul stimuleaza activitatea glycogen sintetazei, stimuleaza captarea aminoacizilor, precum si sinteza unor enzime reglatoare ale gluconeogenezei. La nivelul tesutului muscular striat cortizolul nu pare a avea un efect direct asupra metabolismului glucozei, dar produce rezistenta la insulina prin scaderea ratei la care insulina activeaza sistemul de captare al glucoze. La nivelul tesutului adipos cortizolul determina cresterea lipolizei. Cortizolul inhiba raspunsurile imunologic si inflamator prin alterarea mobilizarii si migrarii leucocitelor, prin scaderea captarii de aminoacizi si glucoza de catre limfocite, prin stabilizarea membranei lizozomiale.
Datorita tuturor acestor efecte cortizolul este considerat un mediator major al raspunsului la agresiune. Acest fapt este intarit si de constatarea ca animalele suprarenalectomizate si pacientii cu boala Addison au o aparare scazuta in conditii de stres. S-a remarcat o crestere a mortalitatii la pacientii critici sedati cu etomidat, etomidatul blocand steroidogeneza la nivelul suprarenalei.
La bolnavul critic, care este supus unui stres prelungit, s-au obsevat valori constant crescute ale cortizolului, explicate de pierderea ritmului circadian a secretiei acestuia. Valorile constant crescute se coreleaza negativ cu evolutia acestor bolnavi. Inhibitia componentelor sistemului imun prin hipercorticismul din starile postagresive poate fi interpretata ca o tentativa de protectie a organismului impotriva unei reactii imun-inflamatorii excesive si potential periculoase.
In concluzie cortizolul este considerat un hormon vital datorita faptului ca deturneaza utilizarea glucozei de la muschi spre creier, faciliteaza actiunea catecolaminelor, contribuind la mentinerea stabilitatii cardiovasculare si previne activarea excesiva a sistemului imun la stres.
Hormonul somatotrop
Hormonul somatotrop denumit si hormon de crestere (growth hormone GH) este sintetizat si eliberat de celulele acidofile ale hipofizei anterioare.
Secretia de GH creste dupa hemoragie ,trauma si anestezie.
La bolnavi in perioada postoperatorie si la cei cu arsuri administrarea de hormon somatotrop a dus la cresterea retentiei azotate, cresterea ratei metabolice si a oxidarii lipidice.
Hormonii tiroidieni
Hormonii tiroidieni tiroxina (T4) si triiodotironina (T3) sunt sintetizati si eliberati de glanda tiroida sub controlul hormonului stimulator tiroidian (TSH) eliberat de celulele basofile ale hipofizei anterioare, ca raspuns la stimularea produsa de hormonul hipotalamic eliberator de tirotropina (TRH).
Bolnavii critici desi prezinta nivele de T3 si T4 scazute au in mod paradoxal hipermetabolism. Scaderea concentratiei de T4 liber la bolnavii critici prezice un prognostic rezervat.
Arginin-vasopresina
Arginin-vasopresina (AVP), denumita in mod clasic hormonul antidiuretic (ADH), este sintetizata in hipotalamus de catre celulele nucleilor supraoptic si paraverntricular de unde este transportata in neurohipofiza unde este stocata pana cand stimulii nervosi produc eliberarea sa.
Exista o multitudine de stimuli ce pot modifica secretia de AVP fie direct prin actiune pe neurohipofiza (durere, emotie, angiotensina II), fie indirect prin modificari ale volumului sanguin, osmolalitatii plasmatice, sau cresterea concentratiei de glucoza (efortul, catecolaminele, opiaceele, insulina, cortizolul, histamina). Majoritatea acestor stimuli apar in timpul agresiunii si in perioada postagresiva asa ca nu este surprinzator faptul ca secretia de AVP este crescuta dupa interventiile chirurgicale majore, sepsis, hemoragie sau arsuri.
Secretia inadecvata de vasopresina este cunoscuta sub denumirea de Sindrom de secretie inadecvata de ADH termen care descrie secretia excesiva de vasopresina peste nevoile impuse de mentinerea homeostaziei. Persistenta secretiei crescute de AVP produce un debit urinar scazut cu urina hiperosmolara si hiponatremie de dilutie.
Situatia inversa este absenta secretiei de AVP, diabetul insipid, caracterizat prin producerea unor cantitati mari de urina diluata in prezenta osmolalitatii plasmatice mult crescute. Aceasta situatie apare mai frecvent la bolnavii comatosi care nu pot sa isi regleze balanta hidrica prin sete si in conditiile mortii cerebrale. Poliuria excesiva conduce la aparitia hipernatremiei plasmatice insotita eventual de hipotensiune arteriala care nu cedeaza decat la administrarea de apa libera si vasopresina exogena.
Gonadotropine
Hormonul stimulator al foliculului (FSH) si hormonul luteinizant (LH) sunt sintetizati si eliberati de adenohipofiza.
S-a constatat suprimarea secretiei de FSH si LH dupa operatii, dupa stres emotional si dupa arsuri. Modificarea secretiei de gonadotropina explica disfunctiile menstruale ce apar frecvent dupa trauma sau stres emotional. in starile postagresive scade si nivelul plasmatic de testosteron.
Oxitocina
Oxitocina este sintetizata in hipotalamus de unde este transportata in hipofiza posterioara. in mod normal eliberata ca raspuns la distensia vaginala, oxitocina poate fi eliberata si ca raspuns la stimuli emotionali, reducerea osmolalitatii plasmatice, hipotensiune si cresterea concentratiei de angiotensina II.
Nu este inca stabilit rolul exact al oxitocinei in cadrul raspunsului neuroendocrin la agresiune.
Prolactina
Prolactina este sintetizata, stocata si eliberata in hipofiza anterioara.
Importanta prolactinei in perioada postagresiva este inca incomplet elucidata, desi au fost remarcate cresteri ale concentratiei plasmatice de prolactina la adulti dupa traume sau operatii, precum si scaderi ale concentratiei plasmatice de prolactina la copii dupa injurie termica.
Opioidele endogene
Opioidele endogene sunt secretate de celule localizate in sistemul nervos central, hipotalamus, lobul intermediar al hipofizei, maduva spinarii, neuronii vegetativi simpatici, si medulara suprarenala.
Opioidele endogene au actiuni diverse: influenteaza perceptia senzoriala, modifica functia cardiovasculara, actioneaza asupra metabolismului intermediar, produce modularea functiilor neuroendocrina si imunologica.
Dupa agresiuni severe (trauma, soc, infectie) s-a remarcat cresterea concentratiei lor.
Hormoni sub control vegetativ
Catecolaminele (adrenalina, noradrenalina, dopamina)
Natura arbitrara a impartirii in sistem nervos si sistem endocrin este pe deplin subliniata de functiile interconectate si supraspuse ale catecolaminelor.
Adrenalina este secretata de catre medulara suprarenala ca raspuns la activarea sistemului nervos simpatic, iar noradrenalina este eliberata in cadrul aceleiasi activari de la nivelul terminatiilor nervoase simpatice. Sistemul nervos simpatic se afla la randul sau sub controlul hipotalamusului, respectiv a acelorasi zone responsabile de secretia factorilor de eliberare si care initiaza si secretia altor hormoni.
Productia si eliberarea de catecolamine este crescuta in numeroase situatii postagresive, mai multi stimuli fiind responsabili de acesta situatie: anxietatea, durerea, hipovolemia, hipoxia, hipoglicemia, hipotensiunea, hipercapnia etc
Dupa traume majore accidentale concentratia plasmatica de adrenalina a fost gasita crescuta numai o perioada scurta de timp (48 ore), pe cand nivelul plasmatic de noradrenalina a ramas crescut pentru 8-l0 zile.
Efectele hemodinamice ale catecolaminelor sunt dependente de doza si constau din: vasoconstrictie venoasa si artreriala mediata de receptorii alfa 1, vasodilatatie arteriala mediata de receptorii beta 2, cresterea contractilitatii miocardice, cresterea ritmului cardiac si cresterea perioadei de recuperare a nodulului sinusal mediate de receptorii beta 1. in doze mici adrenalina actioneaza in primul rand asupra receptorilor beta 1 si beta 2, iar in doze mari actiunea principala sa se manifesta asupra receptorilor alfa-l. in circumstante fiziologice noradrenalina are actiuni beta 1 si alfa. Efectele hemodinamice ale dopaminei sunt mediate de receptorii dopaminergici si de receptorii adrenergeici: in concentratii scazute dopamina produce vasodilatatie renala prin actiune pe receptorii dopaminergici; la concentratii mai mari dopamina are efecte pe receptorii beta 1 si alfa 1.
Nivelul de dopamina este si el crescut in starile posttraumatice, probabil prin eliberarea de la nivelul terminatiunilor libere simpatice. Rolul dopaminei in stres este putin cunoscut in prezent, dar este cert faptul ca nivelul concentratiei plasmatice evolueaza in paralel cu concentratia noradrenalinei.
Insulina
Sinteza si secretia de insulina de catre celulele pancretice beta sunt controlate de: concentratia substratului circulant (glucoza, aminoacizi, acizi grasi liberi), de activitatea sistemuluii nervos vegetativ si de efectul direct sau indirect al unor hormoni.
In conditii normale concentratia plasmatica de glucoza reprezinta cel mai important sistem de control al secretiei de insulina.
In conditii postagresive efectul glicemiei este estompat de mecanisme vegetative si hormonale care produc rezistenta la insulina. Acest fenomen este datorat densitatii mai mari de receptori alfa-adrenergici, decat beta-adrenergici la nivelul celulelor beta pancreatice. Activarea receptorilor alfa adrenergici prin stimularea simpatica si cresterea concentratiilor circulante de adrenalina si noradrenalina, fenomene caracteristice perioadei postagresive, inhiba secretia de insulina. in contrast administrarea de isoproterenol, exclusiv beta agonist adrenergic produce cresterea secretiei de insulina. Stimularea parasimpatica produce deasemenea o crestere a secretiei de insulina.
Eliberarea si activitatea insulinei este suprimata dupa operatie si in timpul fazei acute a injuriei. Acesta este rezultatul efectelor directe pe celulele pancreatice si modificarilor determinate de catecolamine in activitatea insulinei si glucozei. Totusi, spre deosebire de inanitie, nivelul concentratiei plasmatice de insulina este semnificativ crescut fata de nivelul bazal, dar nu suficient de cresctut fata de nivelul glicemiei.
Glucagonul
Sinteza si secretia de glucagon de la nivelul celulelor alfa pancreatice sunt controlate de concentratia substratuli circulant (glucoza, aminoacizi, si acizi grasi), de eferentele sistemului nervos central si sistemului nervos vegetativ, si de actiunea unor hormoni circulanti sau paracrini.
In conditii normale stimulii care deternina eliberarea de glucagon sunt: glucoza, aminoacizii si efortul
Activitatea glucagonulul este importanta in cadrul raspunsului la post si agresiune din cauza efectelor de crestere a productieie hepatice de glucoza si datorita cetogenezei hepatice Cresterea precoce a glicemiei, reducerea secretiei de insulina, cresterea concentratiilor catecolaminelor si cresterea gradata a nivelului de glucagon sunt caracteristici ale raspunsului acut la operatie si agresiune mediate de sistemul nervos vegetativ
Renina - Angiotensina
In conditii fiziologice activitatea reninei prezinta un ritm circadian cu un maximum de activitate seara si noaptea.
In perioada postagresiva se pierde acest ritm circadian si activitatea reninica este constant crescuta pe intreaga perioada de 24 ore. Activitatea reninica crescuta poate fi suprimata in perioada imediat postoperatorie prin administrarea de solutii saline isotone care corecteaza contractia de spatiu extracelular.
In circulatie renina are capacitatea de a converti substratul reninic (angiotesinogenul) sintetizat in ficat in Angiotensina I. Angiotensina I reprezinta precursorul din care se formeaza Angiotensina II la nivelul circulatiei pulmonare sub actiunea enzimei de conversie. Aceasta este un puternic vasoconstrictor, produce o crestere a contractilitatii si frecventei cardiace si creste permeabilitatea vasculara. Tot ea influenteaza si homeostazia hidroelectrolitica prin stimularea puternica a secretiei de aldosteron, prin cresterea secretiei de vasopresina si prin participarea la reglarea mecanismului setei.
Concentratia plasmatica de Angiotensina II creste imediat in perioada postagresiva. in conditiile de scadere a volumului sanguin circulant Angiotensina II contribuie alaturi de catecolamine la redistributia regionala a fluxului sanguin si asigura supravietuirea temporara prin 'centralizarea circulatiei'.
Aldosteron
Secretia de aldosteron creste in perioada postagresiva. in conditii fiziologice productia de aldosteron este controlata de sistemul renina-angiotensina.
Principala actiune a aldosteronului se manifesta asupra metabolismului hidroelectrolitic. El creste reabsorbtia sodiului si secretia de potasiu. Aceste actiuni au un rol dosebit de important in compensarea hipovolemiei realizand un mecanism de reglare inversa dependent de volum.
Peptidele atriale natriuretice.
Peptidele atriale natriuretice (ANP) sunt eliberate de catre sistemul nervos central si de catre granulele neurosecretorii de la nivelul miocitelor atriului stang ca raspuns la modificarea tensiunii peretelui atrial.
ANP contrabalanseaza efectele sistemului renina- angiotensina aldosteron activat in perioada postagresiva.
Somatostatina
Este sintetizata si secretata de celulele delta pancreatice, de unii neuroni centrali si periferici si de multe alte celule. Ea este implicata in homeostazia hidratilor de carbon si functionarea pancreasului endocrin.
Factorii de crestere insulin-like (somatomedinele)
In perioada postagresiva s-a constatat o scadere a concentratiei lor care se coreleaza cu balanta azotata negativa.
Hormonul paratiroid
Hormonul paratiroid (PTH),este sintetizat si eliberat de glandele paratiroide, ca raspuns la modificarea concentratiei serice a calciului ionizat. Rolul exact al PTH in cadrul raspunsului la agresiune nu este inca complet stabilit.
4.2. Raspunsul inflamator
In ultimii 15 ani au aparut numeroase argumente care pledeaza pentru actiunea mediatorilor inflamatiei alaturi de mediatorii neuroendocrini clasici in producerea modificarilor fiziopatologice postagresive.
Raspunsul inflamator local este determinat de o multitudine de factori (distructie tisulara, operatie, infectie sau alte antigene straine) si reprezinta un proces biologic fundamental necesar si indispensabil procesului de reparatie si vindecare.
Identificarea celor patru semne cardinale ale inflamatiei acute : RUBOR, DOLOR, CALOR si TUMOR, a fost facuta de Celsus in primul secol al erei noastre, iar Virchow adauga la sfarsitul secolului trecut cel de al cincelea semn FUNCTIO-LAESA.
Procesul inflamator, excelent descris de Mecinikov inca de la sfarsitul secolului trecut, este considerat un fenomen local pana in urma cu mai putin de doua decenii cand s-a inteles ca inflamatia este o reactie sistemica, care detine un rol major in raspunsul fiziologic la agresiune si care poate fi implicata in anumite conditii in patogenia a numeroase suferinte acute sau cronice.
In consecinta, raspunsul la trauma nu mai poate fi privit doar ca un raspuns neuroendocrin, participarea constanta si integrata a mediatorilor raspunsului inflamator in cadrul raspunsului la agresiune oferind alte dimensiuni fenomenelor care se petrec in perioada posttraumatica.
Factorii care contribuie la elaborarea si dezvoltarea raspunsului inflamator sunt reprezentati de o serie de elemente acelulare si celulare care actioneaza atat local cat si in circulatie.
Elementele acelulare implicate in raspunsul local si sistemic la injuria tisulara sunt reprezentate de patru sisteme de proteine plasmatice, de autacoizii, de citokine si de factorii eliberati de la nivelul celulelor endoteliale. (Tabel 1).
Tabel 1.
Elementele umorale ale raspunsului inflamator.
|
ELEMENTE UMORALE |
|
|
CASCADE ENZIMATICE |
Sistemul activarii de contact Sistemul coagularii Sistemul fibrinolizei Sistemul complementului |
|
AUTACOIZI |
Eicosanoide: - prostaglandinele - leucotrienele Histamina Serotonina Somatomedinele |
|
CITOKINE |
TNF Interleukinele 1,2,6, si 8 etc. Interferon-g |
|
FACTORI ELIBERATI DE CELULELE ENDOTELIALE |
Oxidul nitric Endoteline Prostaglandine Factorul activator plachetar (PAF) |
Elementele celulare ale raspunsului inflamator sunt :
- Mastocitele si bazofilele;
- Sistemul mononuclear fagocitar (Tabel 2);
- Neutrofilele;
- Celulele endoteliale.
Trauma produce rupturi ale capilarelor, vaselor mari si tesuturilor. Capilarele se contracta, apare agregarea intravasculara a plachetelor, este activata coagularea si se formeaza cheagul de fibrina. in functie de caracterul injuriei poate exista si contaminare bacteriana. in primele 48 de ore dupa injurie se dezvolta un proces inflamator la nivelul plagii. Capilarele se dilata si devin permeabile pentru proteinele plasmatice care patrund la nivelul plagii. Leucocitele din sange adera initial la endoteliu vaselor mici (in special venule) iar ulterior trec prin peretele vascular. in scurt timp plaga este infiltrata cu exsudat celular inflamator care contine: leucocite, hematii si fibrina. Extensia si durata procesului este dependenta de amploarea distructiei tisulare, de dimensiunea plagii si de gradul de contaminare bacteriana. Initial proportia de polimorfonucleare si macrofage este egala. Dupa cateva zile numarul polimorfonuclearelor scade iar numarul macrofagelor si monocitelor creste. Rolul polimorfonuclearelor este important si indispensabil doar in conditiile unei plagi contaminate, deoarece plaga aseptica se poate vindeca si in absenta lor. Rolul limfocitelor in vindecarea plagii nu este inca bine precizat. Macrofagele si monocitele sunt elementele celulare indispensabile vindecarii plagii atat prin capacitatea lor de a 'curata' plaga cat si pentru activitatile lor fibroblastice.
In procesul inflamator de la nivelul plagii participa o serie de mediatori. Histamina (din celulele mastocitare, din granulocite si din plachete) si serotonina (din mastocite) sunt puternic vasodilatatoare dar au o durata de viata scurta si deci efectele vor fi tranzitorii. Rolul lor pare a fi important doar in initierea procesului de vindecare a plagii. Sistemul kinin-kalicreina plasmatic (sistemul de contact) si sistemul prostanoid participa deasemenea in procesul inflamator local. Bradikinina produsa si de granulocite este un puternic vasodilatator si creste semnificativ permeabilitatea capilara. Kalidina provenita din alfa2 globulina plasmatica si unele prostaglandine (PGE1, PGE2) contribuie la cresterea permeabilitatii vasculare si creste chemotaxia. Fibronectina, factorul de crestere derivat din plachete leucotrienele apar si ele in procesul inflamator local. Rolul citokinlor in inflamatie este bine documentat astazi. Dintre ele IL1 are ca functie principala stimularea sintezei reactantilor de faza acuta de catre ficat, proteine care migrand la nivelul plagii au rolul de a facilita vindecarea prin controlul inhibitor pe care-l exercita asupra proteazelor leucocitare, prin protectia tesutului impotriva leziunilor autoimune, prin facilitarea productiei aerobe de energie si prin favorizarea sintezei de colagen.
Elementele generate in cadrul procesului inflamator local, in special citokinele de alarma, proinflamatorii, provenite din macrofagele activate (IL-l, IL-6 si TNF), actioneaza si asupra organelor la distanta pe calea unei comunicari directe celula-celula (Tabel 2).
Tabel 2.
Principalele citokine implicate in raspunsul inflamator / catabolic si principalele lor efecte biologice
|
TNF-alfa |
Hipotensiune ARDS Coagulopatie Anorexie Casecsie ? Activare neuroendocrina hipertrigliceridemie rezistenta la insulina sinteza proteinelor de faza acuta gluconeogeneza turnover al a.acizilor si a.grasi Neutropenie |
|
IL-lb |
Hipotensiune (sinergica cu TNF-a) Anorexie Febra Activare neuroendocrina Depresiune a s.n.c. Neutrofilie |
|
IL-2 |
Importanta in raspunsul antigenic Proprietati endotoxin-like |
|
IL-6 |
Sinteza proteinelor de faza acuta Inhiba sinteza TNF-a si IL-lb |
|
IL-8 |
Captarea leucocitelor la locul infectiei |
|
IL-l0 |
Inhiba sinteza TNF-a si IL-lb |
|
Interferon-g |
Sinergic cu TNF-a si alte citokine |
|
CITOKINE |
RASPUNS |
Pentru a sublinia dimensiunea sistemica a efectelor produse la distanta de mediatorii inflamatiei, acestea au fost grupate sub denumirea de Sindrom de raspuns Inflamator Sistemic. (SRIS).
In ultimul deceniu s-au acumulat numeroase date experimentale si clinice care atesta rolul fiziologic si patologic al raspunsului inflamator in cadrul raspunsului la agresiune. SRIS este integrat cu raspunsul neuroendocrin clasic, ambele actionand, in conditii normale, coordonat in scopul vindecarii locale si generale necesare supravietuirii (. 3).
Raspunsul la agresiune este considerat in prezent ca un raspuns imunobiologic complex, implicand, asa dupa cum am aratat, sistemul imunitarinflamator, cascada complementului, sistemul monocitar-fagocitar, impreuna cu o serie de mediatori locali si sistemici, majoritatea eliberati de activarea macrofagelor, monocitelor si celulelor endoteliale, care stimuleaza mecanismele de aparare impotriva leziunilor tisulare si consecutiv impotriva invaziei microbiene. Nivelul acestui raspuns, impreuna cu abilitatea de a controla posibilele complicatii septice joaca un rol fundamental in prognosticul pacientului.
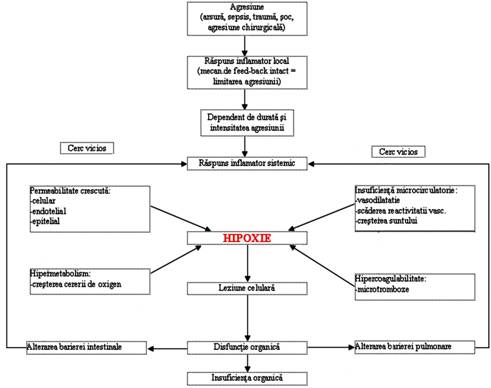
. 3. Interrelatia dintre agresiune, sindrom inflamator local, sindrom inflamator sistemic, disfunctii organice multiple
.
In anumite circumstante deosebite raspunsul inflamator sistemic este exagerat si evolueaza necontrolat, determinand anomalii mari in homeostazie, manifestate clinic prin sepsis sever si Sindrom de Disfunctii Organice Multiple.Aceste circumstante apar atunci cand injuria este suficient de mare pentru a determina pierderea mecanismelor de control, insotita de eliberarea unei cantitati anormal crescute de mediatori sau de activarea sistemica a unor mediatori care in mod obisnuit actioneaza pe o arie restransa.
La bolnavul critic, se descrie si o forma de sindrom inflamator sistemic cronic, ce nu se mai remite si in timp duce la casexie si deces. Un raspuns atenuat duce la vindecare intarziata sau favorizeaza aparitia infectiei.
4.3. Raspunsul celular la agresiune
Pe langa modificarile complexe descrise anterior care se produc la scara intregului organism stresul induce si o serie de modificari celulare si moleculare care fac parte integranta din raspunsul la agresiune.
S-a constatat ca celule de provenienta extrem de diversa au capacitatea de a raspunde intr-o maniera remarcabil de constanta si rapida la modificarile mediului lor inconjurator. Raspunsul celular la agresiune reprezinta de fapt o modalitate eficienta de aparare a celulei impotriva factorilor care-i perturba homeostazia. Suportul molecular al raspunsului consta in transcriptia si translatia rapida a unor proteine intracelulare foarte bine consevate si scaderea productiei celorlalte polipeptide celulare.
In consecinta principalele componente celulare sunt protejate de actiunea ireversibila a agentilor agresori, celula poate supravietui in timpul stresului si se creeaza posibilitatea unei reveniri rapide la activitatile celulare normale in perioada de recuperare.
La organismele pluricelulare, complexe, cum este si organismul uman numerosii agent agresori care pot actiona asupra celulei determina aparitia a doar 4 tipuri de raspuns denumite astfel dupa principalul agresor care induce raspunsul:
- raspunsul la socul caloric;
- raspunsul la stresul oxidativ;
- raspunsul la stresul cu ultraviolete;
- raspunsul de faza acuta.
Raspunsul la socul caloric este cel mai vechi pe scara filogenetica si primul descoperit si reprodus experimental. Celulele mamiferelor sintetizeaza 'proteinele de soc caloric' (HSP = heat shock proteins) in vitro dupa o expunere la temperaturi cu 3-5 grade C mai ridicate decat temperatura normala. Sinteza majorirarii acestor proteine a fost remarcata si in celulele normale 'nestresate' ceea ce indica implicarea lor inca incomplet elucidata in procesele fiziologice celulare. Este cert insa ca sunt esentiale supravietuirii celulare atat in conditii normale cat si de stres.
Raspunsul de faza acuta se deosebeste de celelalte raspunsuri atat prin aparitia sa pe scara filogenetica mult mai tarziu (numai la organismele pluricelulare evoluate) cat si prin complexitatea sa care implica participarea catorva zeci de gene. Raspunsul de faza acuta evolueaza ca un raspuns coordonat al unei mari varietati de celule (celule endoteliale, macrofage, monocite, celule epiteliale) la un agent comun perturbator al homeostaziei. Coordonarea acestui raspuns complex necesita existenta unui sistem rapid si eficient de comunicare intercelulara. Acest sistem de comunicare intercelulara este realizat de citokine, in principal TNF si IL 1. in clinica acest raspuns se manifesta prin scaderea sintezei de albumina si cresterea sintezei de fibrinogen la bolnavii in stare postagresiva.
Exacerbarea acestui raspuns si activarea lui necontrolata se manifesta clinic prin aparitia sindromuli de raspuns inflamator sistemic, predecesorul sindromului de disfunctii organice multiple.
Toate cele 4 raspunsuri celulare la stres au ca element comun modificarile expresiei genelor. Activarea fiecarui raspuns apare initial la nivelul transcriptiei, proces controlat de factorii de transcriptie, care sunt proteine cu secvente specifice legate de ADN. Deoarece factorii de transcriptie sunt relativ limitati initierea unui raspuns specific la stres se poate realiza numai prin activarea unei combinatii particulare de factori. Celulele nu pot executa toate cele patru categorii de raspunsuri concomitent. Cu toate ca fiecare raspuns apare in mod distinct si este caracterizat printr-o anume combinatie de factori de transcriptie s-a constatat ca raspunsurile la anumiti stresori se suprapun partial (. 4).
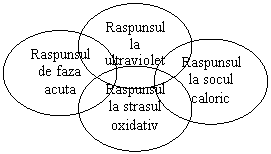
.4. Raspunsul celular la agresiune.
Dintre cele patru categorii de raspunsuri doar raspunsul caloric si raspunsul de faza acuta sunt complet distincte si exclusive. Raspunsul la socul caloric, mai vechi filogenic, are prioritate in fata raspunsului de faza acuta. Mai multe studii experimentale efectuate in vitro si in vivo demonstreaza ca inducerea prealabila a raspunsului la caldura impiedica aparitia raspunsului de faza acuta. in acest fel se poate realiza protectia tranzitorie atat a celulei cat si a organismului din care face parte aceasta impotriva a numerosi agenti agresori care declanseaza raspunsul de faza acuta (sepsis, ischemie, reperfuzie etc.) s-a demonstrat ca stresul caloric premergator instalarii sepsisului la animalele de laborator atenueaza leziunile cardio-pulmonare si amelioreaza sansele de supravietuire. Inducerea experimentala prealabila a raspunsului de faza acuta si expunerea ulterioara la caldura declanseaza, spre deosebire de secventa inversa, un al treilea program de expresie genetica care conduce la apoptosis (moartea programata a celulei). Studii recente incearca insa sa demonstreze experimental ca daca aceasta ultima secventa este foarte stransa raspunsul la socul caloric s-ar putea sa fie cel care domina si isi va exercita in continuare efectul protector atat la nivel celular cat si la nivelul intregului organism. Ce concluzie practica desprind autorii din aceste studii? Ar trebui probabil sa fim mai putin agresivi in combaterea febrei la organismele supuse unei agresiuni endotoxemice.
5. Modificari fizipatologice produse de agresiune
Mediatorii neuroendocrini si imuninflamatori produc in perioada postagresiva imediata o serie de modificari fiziopatologice in scopul restabilirii stabilitatii homeodinamice perturbate de injurie:
Compensare cardiovasculara;
Retentia de apa si sare;
Modificari metabolice;
Vindecarea plagilor;
Imunomodularea.
5.1. Compensarea cardiovasculara
Din punct de vedere cardiovascular trebuie acceptata existenta unui spectru al modificarilor care variaza de la o compensare adecvata pana la disfunctii severe.
Modificarile hemodinamice ce apar in mod obisnuit dupa o interventie chirurgicala de amploare medie (sau o trauma de aceiasi amploare) sunt determinate de necesitatea mentinerii oxigenarii tisulare adecvate in conditiile cresterii consumului de oxigen din perioada postagresiva imediata. Aceasta se realizeaza prin cresterea transportului de oxigen (DO2) si/sau cresterea extractiei periferice de oxigen (ExO2). in perioada postoperatorie imediata DO2 creste rapid prin cresterea debitului cardiac. La un bolnav cu sistem cardiovascular indem DC se poate tripla in perioada imediat postoperatorie. Aceasta marire este asigurata prin cresterea presarcinii ventriculului stang si prin cresterea frecventei cardiace. Posibilitatile de crestere a ExO2 sunt limitate la om la cca. 60%. La o valoare de extractie superioara valorii de 60% consumul de oxigen (VO2) devine dependent de aportul de oxigen (DO2)., care atinge o valoare critica (DO2 critic) care corespunde unei valori de SvO2 de 40%.
Adaptarea la hipovolemie reprezinta o alta modalitate de adaptare a sistemului cardiovascular la agresiune. Raspunsul reflex simpatoadrenergic la hipovolemie declansat de baroreceptori determina o reactie hemodinamica de tip hipodinamic caracterizata prin: venoconstrictie, tahicardie, cresterea fortei de contractie miocardica, cresterea rezistentei vasculare periferice, umplere transcapilara. Aceste modificari de la nivelul macrocirculatiei si de la nivelul microcirculatiei au un sens compensator limitand temporar efectele hipovolemiei prin redistributia regionala a fluxului sanguin (centralizarea circulatiei) si mentinerea unei presiuni arteriale suficiente pentru asigurarea unui flux sanguin coronarian si cerebral adecvat. Persistenta hipovolemiei si implicit a activarii simpatoadrenergice transforma aceasta reactie adaptativa compensatorie in cauza determinanta a producerii disfunctiilor si leziunilor organice prin hipoperfuzie tisulara.
Spre deosebire de reactia adaptativa a sistemului cardiavoscular normal la SRIS sau hipovolemie, sepsisul sever, socul septic si SDOM se caracterizeaza pe hemodinamic printr-un raspuns hiperdinamic care realizeaza o compensare deficitara. Reactia hiperdinamica se manifesta prin scaderea rezistentei vasculare periferice, perturbari grave ale permeabilitatii capilare cu iesirea plasmei in spatiul interstitial, debit cardiac normal sau crescut in ciuda scaderii precoce a contractilitatii miocardice si o concentratie de oxigen crescuta in sangele venos amestecat (SVO2 crescuta) [110;117]. Intr-adevar, compensarea cardiovasculara in timpul stresului chirurgical si a sangerarii controlate terapeutic este eficienta si suficienta pentru a asigura restabilirea homeostaziei si implicit evolutia spre vindecare. Situatia este diferita in prezenta unui raspuns inflamator exagerat determinat de o infectie sau de o trauma severe. in acest context, sistemul cardiovascular este el insusi afectat, iar modificarile hemodinamice isi pierd caracterul compensator si devin inadecvate pentru supravietuire.
In timpul raspunsului inflamator sistemic exagerat (ex. sepsis sever, soc septic SDOM) functia ventriculara este anormala . Desi debitul cardiac este normal sau chiar crescut, fractiile de ejectie ale ambilor ventriculi sunt reduse, iar volumele de la sfarsitul diastolei sunt crescute. Reducerea functiilor ventriculare apare la 24 48 de ore de la debutul agresiunii, si este reversibila la supravietuitori in 5 10 zile dupa revenire. in general, durata starii cardiovasculare hiperdinamice cu reducerea functiei ventriculare va determina prognosticul pacientilor cu sepsis sever. Normlizarea parametrilor hemodinamici in 24 de ore are semnificatia unui prognostic favorabil.
In situatia unui stres chirurgical obisnuit compensarea cardiovasculara normala poate fi influentata de bolile cardiovasculare preexistente, in special de boala coronariana, care poate impiedica desfasurarea elementelor compensatorii.
5.2. Retentia de apa si sare
Actiunea combinata a ADH-ului si aldosteronului determina retentia de apa si sare in scopul mentinerii volumului spatiului extracelular si a volumului intravascular.
Mentinerea volumului spatiului extracelular se realizeaza concomitent cu tendinta la scadere a osmolalitatii. Hiposodemia remarcata si in conditiile unei retentii saline maxime se datoreaza producerii crescute de apa endogena in conditiile hipermetabolismului.
Pe acidobazic exista tendinta la alcaloza metabolica.
Administrarea de solutii glucozate nonelectrolitice in aceasta faza poate produce intoxicatie cu apa prin expandarea concomitenta a spatiului intracelular si a spatiului extracelular.
5.3. Raspunsul metabolic la agresiune
De cate ori organismul este supus unei agresiuni, pe metabolic, apare fenomenul de 'catabolism'. Cuvantul catabolism provine din grecescul katabole ('a da jos') si implica un fenomen generalizat de metabolism destructiv in care tesuturile vii sunt transformate in produsi cu o compozitie chimica mai simpla.
Raspunsul la agresiune se caracterizeaza printr-o accelerare a intregului metabolism al organismului supus la injurie. Acest hipermetabolism este un fenomen generalizat sustinut de o combinatie de eferente umorale si neuro-vegetative proportionale cu intensitatea si severitatea injuriei.
Raspunsul metabolic la agresiune se caracterizeaza printr-o mobilizare rapida a stocurilor energetice si o distrugere a proteinelor cu pierdere concomitenta de azot.
Rezervele nutritionale sunt mobilizate pentru a genera glucoza, amino-acizi si substrat lipidic care sa raspunda nevoilor hipermetabolice ale organismului. Tesutul adipos si glicogenul reprezinta depozitele naturale de glucide si lipide utilizabile ca substrat energetic in caz de inanitie sau steres. Pentru proteine nu exista depozite naturale, asa incat distructia proteinelor reprezinta o pierdere de masa celulara si are repercursiuni asupra functiei organelor. in cazul unui sindrom hipermetabolic post-traumatic prelungit mobilizarea rezervelor metabolice duce la o depletie de proteine esentiale pe langa scaderea rezervelor de grasimi si carbohidrati. in aceste conditii pot sa apara disfunctii majore ale sistemelor de organe. Infectia reprezinta o complicatie frecventa. Daca raman necontrolate aceste fenomene conduc spre insuficiente organice severe si moarte, reprezentand una din principalele cauze de morbiditate si mortalitate postoperatorie.
5.4. Procesul de reparatie tisulara
Vindecarea plagii reprezinta o prioritate biologica si incepe precoce cu toata existenta balantei azotate negative.
Procesele reparatie la nivelul plagii sunt initial anaerobe si impun un mare consum de glucoza ca sursa de energie. Procesul de reparatie tisulara este complex si evolueaza in mod normala in mai multe faze:
- Faza inflamatorie;
- Faza de epitelizare;
- Faza de proliferare;
- Faza de remodelare.
5.5. Imunomodularea
Injuria are capacitatea de a altera rezistenta gazdei prin mai multi factori. Sistemul imunitar este stimulat si deprimat intr-o maniera complexa si inca incomplet elucidata. Sistemul imunitar nespecific este activat: sunt mobilizate si activate la locul injuriei leucocitele circulante si macrofagele, este activat sistemul complementului, este activat sistemul de contact si sistemul opsoninelor, creste sinteza si eliberarea de citokine care activeaza celulele T-helper si promoveaza sinteza si eliberarea proteinelor de faza acuta ca si parte componenta a raspunsului imun. Pe de alta parte, injuriile severe produc o depresie a activitatii leucocitelor si macrofagelor de la nivel hepatic si pulmonar. Hipercatabolismul si malnutritia protein-calorica afecteaza sinteza de imunoglobuline si produce o depresiune a functiilor limfocitelor B si T.
Toti acesti factori contribuie la cresterea susceptibilitatii la infectii. in situatia unei injurii severe si persistente, sistemul imunitar poate fi excesiv activat si devine un factor periculos de autodistrugere tisulara.
Stresul anestezico-chirurgical si morbiditatea postoperatorie
Progresele actuale in anestezie si chirurgie au determinat imbunatatirea semnificativa a evolutiei postoperatorii prin reducerea morbiditatii si mortalitatii si scurtarea duratei internarii in spital.
Cu toate acestea interventiile chirurgicale extensive sunt inca urmate de sechele semnificative, cum ar fi complicatiile cardiace, tromboembolice, pulmonare si infectioase, si implicit de necesitatea spitalizarii postoperatorii indelungate si de cresterea perioadei de convalescenta. Aceste probleme sunt amplificate de cresterea proportiei de bolnavi varstnici si /sau cu boli preexistente severe care sunt acceptati pentru interventii chirurgicale.
Cu exceptia unor defecte de tehnica chirurgicala sau anestezica, patogenia morbiditatii postoperatorii este legata de numeroasele componente ale raspunsul organismului la agresiunea anestezico-chirurgicala.
Din punct de vedere practic exista doua situatii distincte care decid aplicarea masurilor terapeutice de control al raspunsului la agresiune:
a. Chirurgia electiva, in care stimulii care declanseaza raspunsul la agresiune pot fi anticipati si
b. Trauma, infectia si sindromul de disfunctii organice multiple, situatii urgente, in care stimulii raspunsului la agresiune nu pot fi anticipati si preveniti.
a. Chirurgia electiva
Au fost descrisi mai multi factori peri-operatori care impreuna cu raspunsul neuro-hormonal la agresiune pot contribui la morbiditatea postoperatorie, justificand de ce o tehnica chirurgicala impecabila poate duce uneori la o evolutie postoperatorie nefavorabila.
Perioada preoperatorie
Existenta unor suferinte preexistente functionale sau organice reprezinta determinanta majora a mobiditatii si mortalitatii postperatorii.
Depistarea si evaluarea corecta a acestora este posibila numai prin comunicarea si cooperarea intre pacient, internist, chirurg, si anestezist reanimator, aceasta reprezentand cheia succesului in obtinerea celui mai bun prognostic pentru bolnav.
Anxietatea este frecvent intalnita in perioada premergatoare unei interventii chirurgicale. Anxietatea reprezinta o stare emotionala dezagreabila de intensitate variabila putand merge pana la panica. Ea este dificil de obiectivat si masurat, dar pe langa discomfortul pacientului poate influenta calitatea anesteziei si evolutiei postoperatorii.
Afectiunile cardio-vasculare, suferintele pulmonare, sau boala tromboembolica, precum si suferintele altor sisteme de organe agraveaza in mod indubitabil evolutia postoperatorie a bolnavilor.
Abuzul de alcool, chiar inainte de a induce leziuni organice evidente reprezinta un alt factor de risc important. Mecanismele implicate sunt imunosupresia indusa de alcool, disfunctia cardiaca subclinica si un raspuns hormonal amplificat la stresul chirurgical.
Malnutritia reprezinta deasemenea o cauza certa generatoare de patologie postoperatorie, desi este mult mai putin limpede de ce suportul nutritional preoperator nu duce la reducerea scontata a morbiditatii.
Masurile terapeutice aplicate in perioada preoperatorie pentru ameliorarea morbiditatii postoperatorii includ:
Pregatirea psihologica are drept scop eliminarea stimulilor emotionali capabili sa declanseze, asa dupa cum am aratat, raspunsul la agresiune. Realizarea pregatirii psihologice dispune de mijloace nonfarmacologice si de mijloace farmacologice.
Consultul preanestezic reprezinta principala metoda nonfarmacologica care permite reducerea anxietatii preoperatorii.
Dintre mijloacele farmacologice de control al anxietatii, benzodiazepinele sunt preferate altor medicamente (barbiturice, antihistaminice, opioizi), datorita efectului specific eficient si a efectelor secundare ativ mai reduse.
Tratamentul bolilor preexistente
Evaluarea corecta a coexistentelor patologice permite aprecierea predictiva a riscului operator pe baza caruia se poate definii ul terapeutic al ingrijirii perioperatorii care sa scada la maximum morbiditatea posoperatorie . Pe langa pregatirea psihologica si tratamentul bolilor preexistente acest mai trebuie sa cuprinda: profilaxia accidentelor tromboembolice, antibioterapia profilactica adecvata, ificarea adecvata a mijloacelor de monitorizare si terapie intensiva intraoperatorie, stabilirea tacticii chirurgicale.
Perioada intra-operatorie
Pentru a diminua posibilele efecte nedorite ale agresiunii chirurgicale, in perioada intraoperatorie trebuie adoptate o serie de masuri care pot fi grupate in :
- Masuri care scad efectele agresiunii traumatice;
- Masuri care moduleaza stresul neuroendocrin.
Masuri care scad efectele agresiunii traumatice
Evitarea pierderilor sanguine intraoperatorii printr-o tehnica chirurgicala adecvata reprezinta un alt element controlabil care participa la scaderea morbiditatatii postoperatorii.
Dezvoltarea tehnicilor chirurgicale si aparitia in practica de rutina a unor tehnologii noi (ex. chirurgia laparoscopica) care determina scaderea componentei inflamatorii a raspunsului la agresiune a facut posibila introducerea conceptului de chirurgie stress free. Realitatea actuala pune sub semnul intrebarii afirmatia clasica care stipula 'incizie mare, chirurg mare'.
Validarea acestui concept este ilustrata de ameliorarea evolutiei postoperatorii, care a permis ca interventii chirurgicale care necesitau spitalizare de cateva zile in urma cu cativa ani sa poata fi executate astazi in ambulator.
Masuri care moduleaza stresul neuroendocrin
Anestezia moderna si analgezia perioperatorie sunt elemente majore care scad raspunsul la agresiune si au permis efectuarea unor interventii chirurgicale extensive cu o incidenta redusa a complicatiilor postoperatorii.
Notiunea de anestezie stress free a devenit o realitate prin posibilitatile noi de control al componentelor patrulaterului anestezic: analgezie, amnezie/hipnoza, relaxare musculara si asigurarea homeostaziei.
Desi componentele farmacologicie ale tehnicilor de anestezie generala nu influenteaza major raspunsul neurohormonal postoperator, asocierea unor blocaje nervoase regionale (ex. bloc peridural continuu) intrerup aferentele nervoase si produc o scadere a raspunsului hipercatabolic postoperator.
Asigurarea homeostaziei intraoperatorii cuprinde toate tehnicile de supraveghere si terapie intensiva. Aplicarea corecta a unor tehnologii adecvate de monitorizare permite instituirea masurilor terapeutice care controleaza unii stimuli primari ai raspunsului la agresiune (hipovolemia, hipoxia, hipercapnia, acidoza, hipotermia) si scad implicit amploarea raspunsului.
Perioada postoperatorie
Morbiditatea postoperatorie este influentata de factori ca: durerea postoperatorie, greata si varsaturile, hipoxemia postoperatorie, imobilizarea la pat, tulburarile de somn aparute dupa interventii chirurgicale.
Durerea postoperatorie (DPO) este frecventa, cicatrizarea producand o durere de tip inflamator cu o participare hiperalgica, cu o durata medie de 5-7 zile. Dupa numeroase studii incidenta DPO severa si foarte severa este de 50%, controlul terapeutic al acesteia fiind de multe ori insuficient. Pentru interventiile chirurgicale mici si mijlocii analgezia se poate realiza prin abord multimodal utilizand anestezice locale la locul inciziei si administrarea sistemica de paracetamol, antiinflamatoare nonsteroide non aspirinice (NSAID) si opioide intermediare: codeina, dextropropoxiphene, sau tramadol. Nu isi mai gasesc locul in tratamentul actual al durerii postoperatorii aspirina, antispasticele si noramidopirina. Pentru durere postoperatorie severa se recomanda in primul rand tehnici de anestezie regionala: blocaje regionale centrale cu anestezic local si morfinic (rahianestezie, peridurala), blocaje de plex (ex. blocaj de plex axilar) sau blocaje de nervi periferici (ex. blocaj de nervi intercostrali, analgezie intrapleurala). O alternativa inca frecvent utilizata, desi mai putin eficienta, este administrarea sistemica de opioide puternice ca morfina, sau agonisti/antagonisti ca nalbufina sau buprenorfina.
Greata, varsaturile si ileusul sunt printre cele mai comune fenomene postoperatorii. Pe langa neplacerea pe care o provoaca, reprezinta factori determinanti ai recuperarii postoperatorii, deoarece impiedica alimentatia enterala precoce, care reduce complicatiile infectioase postoperatorii si reduce in acelasi timp catabolismul. Tratamentul recomandat pentru greata si varsaturile postoperatorii include utilizarea antiemeticelor: droperidol, propofol, dexametazona si cu efectul cel mai eficient antagonistii receptorilor de tip3 ai serotoninei (ondansteron, dolasetron) in asociere cu tratamentul antalgic eficient cu anestezicelor locale si NSAID si evitarea folosirii morfinicelor. Utilizarea periduralei continue cu anestezice locale are, pe langa efectul analgetic eficient, si un efect de combatere a ileusului postoperator, facilitand in acest fel nutritia enterala precoce si recuperarea postoperatorie.
Hipoxemia postoperatorie imediata, in salonul de trezire, se datoreaza actiunii reziduale a relaxantelor musculare, a opioidelor sau chiar concentratiile reziduale ale anstezicelor volatile. Hipoxemia postoperatorie constanta apare frecvent dupa chirurgia abdominala majora si dureaza 2-5 zile. Pe fondul hipoxemiei constante se supraadauga episoade de agravare ce apar in special noaptea, cu frecventa crescuta in a doua si a treia noapte postoperator. Mecanismul hipoxemiei constante este in principal shuntul pulmonar determinat de reducerea capacitatii reziduale functionale. Desaturarea episodica nocturna este asociata cu tulburarile patternului somnului. Tratamentul hipoxemiei postoperatorii precoce presupune supravegherea adecvata in salonul de postoperator (trezire), pulsoximetru fiind obligatoriu. in functie de cauza producatoare se intervine cu droguri antagoniste sau se apeleaza la suportul ventilator. Oxigenoterapia este obligatorie in perioada imediat postoperatorie.
b. Situatiile de urgenta
Un mare numar de pacienti sufera de agresiuni acute care nu pot fi anticipate si prevenite. Complicatiile infectioase, accidentele traumatice,. insuficientele acute hepatice si renale sunt situatii in care nu exista posibilitatea interventiei inaintea injuriei, masurile terapeutice trebuind a fi initiate, in cel mai bun caz, odata cu inceperea procesului patologic.
In toate aceste situatii pacientii necesita in primul rand interventii terapeutice specifice, ca, resuscitarea cardio-respiratorie, tratamentul leziunilor traumatice, drenajul focarelor infectioase, antibioterapie.
Aceste masuri terapeutice odata instituite vor fi urmate de masurile terapeutice caracteristice perioadelor intra si post injurie.
Pentru majoritatea obiectivelor diagnostice este suficienta testarea sensibilitatii la intepare, atingere, pozitionare si vibratie la nivelul tuturor [...] |
TRATAMENTUL INITIAL Dexametazona, 32 48 mg/zi divizata in 4 6 doze, reduce edemul cerebral datorat tumorii. Poate fi necesara restrictia de aport lich [...] |
Motilitatea corpului este asigurata de neuronii motori centrali si periferici in care primul este un ordonator si eliberator al motilitatii voluntare, [...] |
Copyright © 2010 - 2025
: eSanatos.com - Reproducerea, chiar si partiala, a materialelor de pe acest site este interzisa!
Informatiile medicale au scop informativ si educational. Ele nu pot inlocui consultul medicului si nici diagnosticul stabilit in urma investigatiilor si analizelor medicale la un medic specialist.
Termeni si conditii - Confidentialitatea datelor - Contact